
题目列表(包括答案和解析)
(26分) (1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
① 沉淀 A、B的成分分别是 、 ;步骤②中的试剂a是 ;
② 试写出步骤③中发生反应的离子方式 、 ;
③简述检验所得滤液甲中存在Fe3+的操作方法:__________ _。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
① 加热酸溶过程中发生反应的化学方程式有: 。
② 氧化剂A可选用 (填编号,下同)。
A.KMnO4 B. HNO3 C. Cl2
③ 要得到较纯的产品,试剂B可选用 。
A. NaOH B. CuO C.FeO
④ 试剂B的作用是 。
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
⑤ 从滤液经过结晶得到氯化铜晶体的方法是 (按实验先后顺序选填编号)。
A. 过滤 B. 蒸发至干 C. 冷却 D. 蒸发浓缩
(12分)、A、B、C、D为三种不同的配合物,它们的化学式都是CrCl3·6H2O,但颜色不同: A呈亮绿色,13.325g跟足量AgNO3溶液反应,得到了14.35沉淀;B呈暗绿色,能沉淀1/3的氯;而C呈紫色,可沉淀出全部氯元素;D的溶液跟足量AgNO3溶液不反应,将D在一定温度下,加热分解测得质量减少20.26%。
(1)则它们的结构简式分别为:
A ,B ,C , D 。
2)请画出A结构图。
(6分)、右图是研究外界因素对过氧化氢分解反应速率影响的实验装置图。某学生研究小组在50mL量筒中盛满水,倒置于水槽中,通过分液漏斗把过氧化氢溶液加入锥形瓶中(内中已有适量二氧化锰催化剂),记录各时间段在室温下收集到的氧气的体积。
第1组:粉末状的二氧化锰0.2g+ 5ml 6% H2O2
第2组:粉末状的二氧化锰0.2g+ 3ml 12% H2O2
第3组:粉末状的二氧化锰0.1g+ 5ml 6% H2O2[来源:ZXXK]
第4组:颗粒状的二氧化锰0.1g+ 5ml 6% H2O2
| 催化剂:MnO2 | 第1组 | 第2组 | 第3组 | 第4组 |
| 前15s产生氧气的量(ml) | 11 | 15 | 8 | 7 |
| 前30s产生氧气的量(ml) | 21 | 24 | 11 | 9 |
| 前45s产生氧气的量(ml) | 31 | 35 | 18 | 12 |
| 前60s产生氧气的量(ml) | 45 | 48 | 26 | 15 |
(1)写出H2O2分解的反应方程式: ;
(2)从实验的几组数据中能得到的是: ;
(3)实验比较反应速率时可以测定相同时间内产生气体的体积,也可测 。
(26分)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol·L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响。 |
| ② |
|
|
| |
| ③ |
|
|
| |
| ④ |
|
|
|
(2)实验①中CO2质量随时间变化的关系见下图:
请在图中画出实验②和④中CO2质量随时间变化关系的预期结果示意图。
(26分) (1)铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下: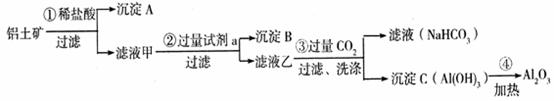
① 沉淀 A、B的成分分别是 、 ;步骤②中的试剂a是 ;
② 试写出步骤③中发生反应的离子方式 、 ;
③简述检验所得滤液甲中存在Fe3+的操作方法:__________ _。
(2)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作: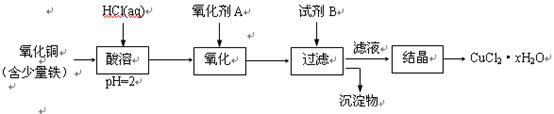
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
① 加热酸溶过程中发生反应的化学方程式有: 。
② 氧化剂A可选用 (填编号,下同)。
A.KMnO4 B. HNO3 C. Cl2
③ 要得到较纯的产品,试剂B可选用 。
A. NaOH B. CuO C.FeO
④ 试剂B的作用是 。
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
⑤ 从滤液经过结晶得到氯化铜晶体的方法是 (按实验先后顺序选填编号)。
A. 过滤 B. 蒸发至干 C. 冷却 D. 蒸发浓缩
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com