
题目列表(包括答案和解析)
下列实验操作中所用的仪器合理的是
A.用25 mL的碱式滴定管量取14.80 mL的KMnO4溶液
B.用100 mL的量筒量取5.2 mL盐酸
C.用托盘天平称取25.20 g氯化钠
D.用250mL的容量瓶配制所需的220mL 0.1mol·L-1的NaOH溶液
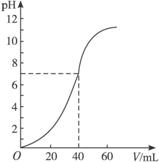
A.1 mol·L-1,100 mL B.0.5 mol·L-1,80 mL
C.1 mol·L-1,60 mL D.1 mol·L-1,80 mL
下列实验操作中所用的仪器合理的是
A.用100 mL的量筒量取5.2 mL盐酸
B.用25 mL的碱式滴定管量取14.80 mL的NaOH溶液
C.用托盘天平称取25.20 g氯化钠
D.用100 mL容量瓶配制50 mL 0.1 mol/L的H2SO4溶液
| |||||||||||||||||||||||||||||||||||||||||
|
用NA表示阿伏加德罗常数的数值,下列说法正确的是 | |
| [ ] | |
A. |
常温下,1 mol D2O含质子数为12 NA |
B. |
在100 mL 0.5 mol/L盐酸中含有HCl分子0.05NA |
C. |
标准状况下,1L水中所含分子数为 |
D. |
15.6 g Na2O2与过量CO2反应时,转移的电子数为0.2 NA |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com