
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
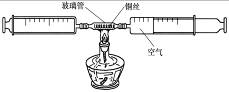
Ôڲⶨ¿ÕÆøÖÐÑõÆøº¬Á¿µÄʵÑéÖУ¬Ð¡Ç¿²ÉÓÃÁËÓÒͼËùʾװÖãºÔÚÓÉÁ½¸ö×¢ÉäÆ÷×é³ÉµÄÃܱÕϵͳÖÐÁôÓÐ25mL¿ÕÆø£¬¸ø×°ÓÐϸÍË¿µÄ²£Á§¹Ü¼ÓÈÈ£¬Í¬Ê±»ºÂýÍƶ¯Á½¸ö×¢ÉäÆ÷»îÈû£¬ÖÁ²£Á§¹ÜÄÚµÄÍË¿Ôڽϳ¤Ê±¼äÄÚÎÞ½øÒ»²½±ä»¯Ê±Í£Ö¹¼ÓÈÈ£¬´ýÀäÈ´ÖÁÊÒΣ¬½«ÆøÌåÈ«²¿ÍÆÖÁÒ»¸ö×¢ÉäÆ÷ÄÚ£¬¹Û²ìÃܱÕϵͳÄÚ¿ÕÆøÌå»ý±ä»¯¡£
(1)ÔÚʵÑé¼ÓÈȹý³ÌÖУ¬½»Ì滺ÂýÍƶ¯Á½¸ö×¢ÉäÆ÷»îÈûµÄÄ¿µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)д³ö¸ÃʵÑéÖз´Ó¦µÄ»¯Ñ§·½³Ìʽ¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)Сǿ²âµÃʵÑé½á¹ûÈçÏ£º
·´Ó¦Ç°×¢ÉäÆ÷ÄÚÆøÌå×ÜÌå»ý | ·´Ó¦ºó×¢ÉäÆ÷ÄÚÆøÌå×ÜÌå»ý |
25mL | 22mL |
ÓÉ´ËÊý¾Ý¿ÉÒÔÍÆËã³öËû²â¶¨µÄ¿ÕÆøÖÐÑõÆøµÄÌå»ý·ÖÊý¡¡¡¡¡¡¡¡¡¡¡¡ 2l£¥(Ìî¡°>¡±¡¢¡°£½¡±¡¢ ¡°<¡±)¡£Ôì³É¸ÃʵÑé³öÏÖÎó²îµÄÔÒò¿ÉÄÜÊÇ¡¡¡¡¡¡¡¡¡¡ ¡£(ÌîÐòºÅ)
¢ÙûÓн»Ì滺»ºÍƶ¯Á½¸ö×¢ÉäÆ÷»îÈû£»¢Ú¶ÁÊýʱûÓÐÀäÈ´ÖÁÊÒΣ»¢Û¼ÓÈëÍË¿Á¿Ì«ÉÙ£»¢Ü¼ÓÈëÍË¿Á¿Ì«¶à
(4)ͨ¹ýÉÏÃæµÄʵÑ飬Äãѧµ½µÄ²âÁ¿»ìºÏÎïÖÐij³É·Öº¬Á¿µÄ·½·¨ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
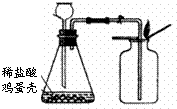
| ¡¡¡¡´Î¡¡Êý | µÚ1´Î | µÚ2´Î | µÚ3´Î | µÚ4´Î | µÚ5´Î |
| ¼ÓÈëÏ¡ÑÎËáµÄÖÊÁ¿£¨g£© | ¡¡¡¡2l | ¡¡¡¡21 | ¡¡¡¡2l | ¡¡¡¡2l | ¡¡¡¡21 |
| Ê£Óà¹ÌÌåµÄÖÊÁ¿£¨g£© | ¡¡¡¡16 | ¡¡¡¡12 | ¡¡¡¡8 | ¡¡¡¡4 | ¡¡¡¡4 |
| ||
| ¡÷ |
| ||
| ¡÷ |
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com