
题目列表(包括答案和解析)
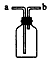
在一次化学研究性学习实验中,某研究小组学生,研究分析某两瓶无标签的试剂,只知道一瓶是固体,另一瓶是液体,取少量两种试剂在试管中混合,立即产生一种无色无味的气体。现请你对此气体开展一系列探究,并完成下列实验报告。
(1)①此气体是什么物质(只写出其中可能的一种)?验证它的实验方案如下:
猜想 | 实验步骤 | 现象及结论 |
此气体可能是____ | _________________________ ________________________ | ____________ _____________ __ |
产生此气体的化学方程式可能是___________________________.
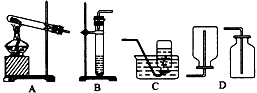
②想制取该气体,采用的发生装置可选用如下图中的__________ (对应填序号)。收集该气体可选用D中的某一个装置。

③若右图是收集该气体的装置,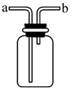
气体由 端(填“a”或“b”)导入。
(2)猜想此无色气体还有无可能是另一种气体,如果有,请写出产生它的化学方程式______ 只须写一种)。
在一次化学研究性学习实验中,某研究小组学生,研究分析某两瓶无标签的试剂,只知道一瓶是固体,另一瓶是液体,取少量两种试剂在试管中混合,立即产生一种无色无味的气体。现请你对此气体开展一系列探究,并完成下列实验报告。
(1)①此气体是什么物质(只写出其中可能的一种)?验证它的实验方案如下:
| 猜想 | 实验步骤 | 现象及结论 |
| 此气体可能是____ | __ |
产生此气体的化学方程式可能是___________________________
②想制取该气体(用本题中两瓶无标签的试剂),采用的发生装置可选用下图A、B、C中的__________ (对应填序号)。收集该气体可选用D中的 装置。


③若下图E是收集该气体的装置,气体由 端(填“a”或“b”)导入。

E
(2)猜想此无色气体还有无可能是另一种气体,如果有,
请写出产生它的化学方程式______ __ ___(只须写一种)。
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液 的体积(mL) |
20.05 | 20.00 | 18.80 | 19.95 |
| 醋酸浓度 (mol?L-1) |
0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol?L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 ③ ③ 探究温度对该反应速率的影响;(Ⅲ)实验①和 ④ ④ 探究大理石规格(粗、细)对该反应速率的影响. |
| ② | ||||
| ③ | ||||
| ④ |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com