金属材料在生产、生活中的应用非常广泛.
(1)铁制品锈蚀的过程,实际上是铁与空气中的氧气、
水蒸气
水蒸气
等发生化学反应的过程.写出防止铁制品锈蚀的一种方法:
在铁制品表面涂油
在铁制品表面涂油
.
(2)若铁矿石选用赤铁矿(主要成分是氧化铁),表示炼铁原理的化学方程式为
.
用1000t含铁56%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是
A
A
(选填序号).
A.583.3t B.560t C.408.3t D.392t
(3)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铁、铜的金属活动性顺序进行验证.
①方法一所选用的3种物质是
铁片
铁片
、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的3种物质是锌片、铜片和
硫酸亚铁溶液
硫酸亚铁溶液
.
③方法三所选用的4种物质是锌片、铁片、铜片和稀硫酸,能验证锌、铁、铜的金属活动性顺序的实验现象是
铜与稀硫酸不反应,锌、铁均能与稀硫酸反应产生气体,且锌的反应比铁剧烈
铜与稀硫酸不反应,锌、铁均能与稀硫酸反应产生气体,且锌的反应比铁剧烈
.
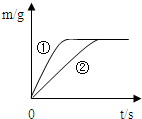
(4)将27g铝粉、56g铁粉分别与等量的同种稀硫酸充分反应,生成氢气的质量(m)与反应时间(t)的关系如右图所示.下列叙述与该曲线图相符的是
CD
CD
(选填序号).
A.①表示铁粉与稀硫酸反应的情况
B.反应结束,铝、铁均完全反应,硫酸有剩余
C.反应结束,硫酸完全反应,铝、铁均有剩余
D.反应结束,硫酸、铁均完全反应,铝有剩余.

 B、铝蒸锅
B、铝蒸锅 C、钢导线
C、钢导线
 金属材料在生产、生活中的应用非常广泛.
金属材料在生产、生活中的应用非常广泛.