
题目列表(包括答案和解析)
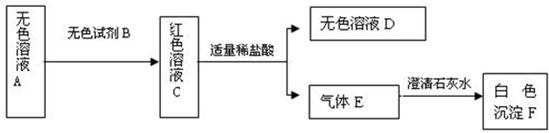
 如图A、B、C、D、E是初中化学常见的五种基本物质.且A、B、C、D都含有一种相同的元素.其中C俗称小苏打,D为食盐的主要成份,A、E发生中和反应,图中“-”表示两端的物质之间能发生化学反应,“→”表示物质间存在转化关系;部分反应物和生成物已略去.根据图示关系和所给条件完成下列各题.
如图A、B、C、D、E是初中化学常见的五种基本物质.且A、B、C、D都含有一种相同的元素.其中C俗称小苏打,D为食盐的主要成份,A、E发生中和反应,图中“-”表示两端的物质之间能发生化学反应,“→”表示物质间存在转化关系;部分反应物和生成物已略去.根据图示关系和所给条件完成下列各题.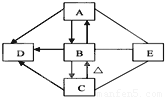
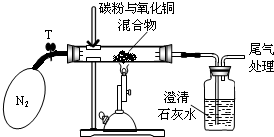 某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.| 操作步骤及实验现象 | 简答 |
| ①称取8g氧化铜与2g碳粉均匀混合,放入重48.4g的玻璃管中,按上图装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是 |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 澄清石灰水变浑浊的化学方程式为: |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为56.0g | / |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com