ЫсгъЪЧpHаЁгк5.6ЕФНЕЫЎЃЎЮвЙњДѓВПЗжЕиЧјЫљНЕЫсгъжївЊЪЧгЩОгУёКЭЙЄГЇШМЩеКЌСђЕФУКвдМАФГаЉЛЏЙЄГЇЩњВњЙ§ГЬжаХХЗХЕФЖўбѕЛЏСђЦјЬхЃЌОЙ§вЛЯЕСаЛЏбЇЗДгІЖјаЮГЩЕФЃЎ
ЃЈ1ЃЉШчЙћСђЗлдкбѕЦјжаШМЩеЃЌЙлВьЕНЕФЯжЯѓЪЧ
ОчСвШМЩеЃЌЗХГіШШСПЃЌВњЩњУїССЕФРЖзЯЩЋЛ№бцЃЌВњЩњвЛжжЮоЩЋгаДЬМЄадЦјЮЖЕФЦјЬх
ОчСвШМЩеЃЌЗХГіШШСПЃЌВњЩњУїССЕФРЖзЯЩЋЛ№бцЃЌВњЩњвЛжжЮоЩЋгаДЬМЄадЦјЮЖЕФЦјЬх
ЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ
ЃЎ
ЃЈ2ЃЉМИЮЛЭЌбЇЮЊСЫЬНОПФОЬПжаЪЧЗёКЌгаЩйСПСђдЊЫиЃЌЫћУЧЩшМЦСЫШчЭМ1ЫљЪОЪЕбщНјааВтЖЈЃЎЧыаДГіЭМжавЧЦїaЕФУћГЦЃК
лсліЧЏ
лсліЧЏ
ЃЎЫћУЧВщдФзЪСЯКѓЕУжЊЃКЁАЖўбѕЛЏСђФмЪЙK
2Cr
2O
7ШмвКЭЪЩЋЃЈгЩГШКьЩЋБфГЩТЬЩЋЃЉЃЌЗДгІЗНГЬЪНЮЊЃКЁА3SO
2+K
2Cr
2O
7+H
2SO
4ЈTK
2SO
4+

+H
2OЁБЃЎШЛЖјЛЏбЇЗНГЬЪНжагавЛЩњГЩЮяВЛЧхГўЃЌЧыИљОнвббЇжЊЪЖЭЦВтЦфЛЏбЇЪНЃК
Cr2ЃЈSO4ЃЉ3
Cr2ЃЈSO4ЃЉ3
ЃЎЗДгІЧАK
2Cr
2O
7жаCrдЊЫиЛЏКЯМлЮЊ
+6
+6
МлЃЎ
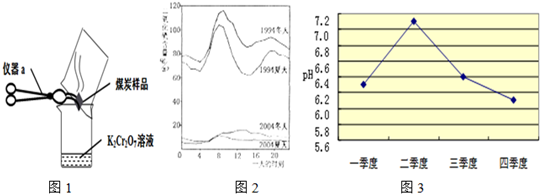
ЃЈ3ЃЉШчЭМ2ЪЧ1994ФъКЭ2004ФъФГГЧЪаЕФвЛЬьИїИіЪБПЬВтЕНЕФПеЦјжаЖўбѕЛЏСђЕФКЌСПЃЎЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
D
D
AЃЎЧњЯпЯдЪОЖЌЬьДѓЦјжаЕФЖўбѕЛЏСђКЌСПБШЯФЬьИп
BЃЎЧњЯпЯдЪОСЫ1994ФъвЛЬьжаДѓдМ8ЕузѓгвЖўбѕЛЏСђЕФКЌСПНЯИп
CЃЎЖўбѕЛЏСђЕФКЌСПдк10ФъМфНЕЕЭЕФдвђПЩФмЪЧМгЧПСЫШМСЯЕФЭбСђКЭПижЦСЫЖўбѕЛЏСђЕФХХЗХ
DЃЎЖўбѕЛЏСђЮлШОЕФжївЊРДдДЪЧЦћГЕХХЗХЕФЮВЦјЃЌПижЦЮлШОЕФЗНЗЈЪЧНћжЙЪЙгУЦћГЕ
ЃЈ4ЃЉдкбаОПЫсгъЮЃКІЕФЙ§ГЬжаЃЌВтЖЈИУЕиЧјгъЫЎЕФpHЕФЪЕбщВйзї
гУВЃСЇАєеКШЁгъЫЎЃЌЕудкЪджНЩЯЃЌгыБъзМБШЩЋПЈЖдееЃЌЖСШЁЪ§жЕ
гУВЃСЇАєеКШЁгъЫЎЃЌЕудкЪджНЩЯЃЌгыБъзМБШЩЋПЈЖдееЃЌЖСШЁЪ§жЕ
ЃЎ
ФГЛЏбЇаЫШЄаЁзщШЁИеНЕЕНЕиУцЕФгъЫЎЃЌУПИєвЛЖЈЪБМфгУНЯОЋУмЕФpHМЦВтЖЈЦфpHЃЌЪ§ОнШчЯТЃК
| ВтЖЈЪБМф/Зжжг |
0 |
1 |
2 |
3 |
| pH |
4.73 |
4.62 |
4.56 |
4.55 |
гЩДЫПЩжЊИУгъЫЎЕФЫсаддНРДдН
ЧП
ЧП
ЃЈЬюЁАЧПЁБЛђЁАШѕЁБЃЉЃЌзюжеЧїгкЮШЖЈЃЎПЩФмЕФдвђЪЧгъЫЎжаЕФH
2SO
3БЛбѕЦјбѕЛЏЮЊH
2SO
4ЃЌЛЏбЇЗНГЬЪНЮЊ
2H2SO3+O2=2H2SO4
2H2SO3+O2=2H2SO4
ЃЎ
ЃЈ5ЃЉЫсгъдьГЩЕФЮЃКІКмЖрЃЎФГаЫШЄаЁзщЕїВщЗЂЯжФГЪаЕФЪЏПЬЕФБэУцгаВЛЭЌГЬЖШЕФИЏЪДЃЎЧвНќ20ФъЕФИЏЪДЫйЖШДѓДѓГЌЙ§вдЭљЃЌЦфжазюжївЊдвђжЎвЛОЭЪЧЫсгъЃЎЮЊСЫМѕЛКЪЏПЬИЏЪДЃЌЧыФуЬсвЛЬѕНЈвщЃК
ЪЙгУЧхНрФмдД
ЪЙгУЧхНрФмдД
ЃЎЫсгъЛсЪЙКгСїЁЂКўВДЫсЛЏЃЎШчЭМ3ЪЧФГЪаШЅФъФГКгСївЛФъжаВЛЭЌЪБЦкКгЫЎЕФЦНОљpHБфЛЏЕФелЯпЭМЃЎдђШЅФъКгЫЎЫсадзюЧПЕФМОЖШЪЧЕк
ЫФ
ЫФ
МОЖШЃЎИУМОЖШгъЫЎЫсадзюЧПЕФдвђПЩФмЪЧЃКЃЈД№СНЬѕЃЉ
ЖЌМОШЁХЏЃЌашвЊШМЩеДѓСПЛЏЪЏШМСЯЃЌМгДѓСЫЖдКгЫЎЕФЮлШО
ЖЌМОШЁХЏЃЌашвЊШМЩеДѓСПЛЏЪЏШМСЯЃЌМгДѓСЫЖдКгЫЎЕФЮлШО
ЃЛ
ЖЌМОНЕЫЎСПМѕЩйЃЌКгЫЎжаЫсЕФХЈЖШдіДѓ
ЖЌМОНЕЫЎСПМѕЩйЃЌКгЫЎжаЫсЕФХЈЖШдіДѓ
ЃЎ
ЫсгъЛЙЛсЪЙЭСШРЫсЛЏЃЎЮЊСЫжаКЭЫсадЭСШРЃЌПЩвдЪЙгУЪьЪЏЛвЗлФЉЃЌШєИУЫсгъЕФГЩЗжЪЧСђЫсЃЌЧыаДГіИУжаКЭЗДгІЕФЛЏбЇЗНГЬЪН
H2SO4+CaЃЈOHЃЉ2=CaSO4+2H2O
H2SO4+CaЃЈOHЃЉ2=CaSO4+2H2O
ЃЎ
ЃЈ6ЃЉФГаЃЛЏбЇаЫШЄаЁзщдкбЇЭъМюЕФЛЏбЇаджЪКѓЃЌЯыЕНгУNaOHШмвКЮќЪеSO
2ЃЌЗДгІЛЏбЇЗНГЬЪНШчЯТЃК2NaOH+SO
2ЈTNa
2SO
3+H
2O гУNaOHШмвКЮќЪе1000LвбГ§ШЅCO
2ЕФПеЦјбљЦЗЃЌШмвКжЪСПдіжиСЫ0.64gЃЎвбжЊДЫЪБПеЦјЕФУмЖШдМЮЊ1.3g/LЃЌЧѓЃК
ЂйБЛЮќЪеЕФSO
2ЕФжЪСП
0.8
0.8
gЃЎ
ЂкЗЂЩњЗДгІЕФNaOHЕФжЪСПЃЎЃЈЯрЖддзгжЪСПЃКNa-23 S-32 O-16ЃЉ
ЂлПеЦјжаSO
2ЕФжЪСПЗжЪ§ЃЈМЦЫуНсЙћОЋШЗЕН0.01%ЃЉЃЎ

 ( )
( ) ЕЫЎзЪдДНєШБЕФдвђжЎвЛЪЧШЫРрЕФЩњВњЁЂЩњЛюдьГЩСЫЫЎЕФЮлШОЃЎФГГЧеђЩњВњЁЂЩњЛюЧјЕФЗжВМШчЯТЭМЫљЪОЃЎКгСїжаAЁЂBЁЂCШ§ДІФГДЮЫЎбљГщВтНсЙћШчБэЫљЪОЃЎ
ЕЫЎзЪдДНєШБЕФдвђжЎвЛЪЧШЫРрЕФЩњВњЁЂЩњЛюдьГЩСЫЫЎЕФЮлШОЃЎФГГЧеђЩњВњЁЂЩњЛюЧјЕФЗжВМШчЯТЭМЫљЪОЃЎКгСїжаAЁЂBЁЂCШ§ДІФГДЮЫЎбљГщВтНсЙћШчБэЫљЪОЃЎ
 +H2OЁБЃЎШЛЖјЛЏбЇЗНГЬЪНжагавЛЩњГЩЮяВЛЧхГўЃЌЧыИљОнвббЇжЊЪЖЭЦВтЦфЛЏбЇЪНЃК
+H2OЁБЃЎШЛЖјЛЏбЇЗНГЬЪНжагавЛЩњГЩЮяВЛЧхГўЃЌЧыИљОнвббЇжЊЪЖЭЦВтЦфЛЏбЇЪНЃК