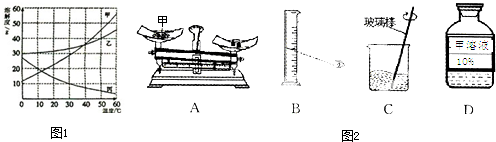
甲、乙、丙三种固体物质的溶解度曲线如图1所示.
(1)30℃时,丙的溶解度是
10g
10g
.
(2)20℃时,甲、乙、丙三种物质的溶解度按由大到小的顺序排列的是
乙>甲>丙
乙>甲>丙
.
(3)欲将20℃时丙不饱和溶液变为饱和溶液,可采用的方法是
加入丙(或恒温蒸发溶剂)
加入丙(或恒温蒸发溶剂)
(写出一种即可).
(4)5℃时,取甲、乙、丙三种固体物质各20g分别加入盛有100g水的烧杯中,充分搅拌后得到的溶液,能够饱和的是
甲
甲
物质的溶液.又将三个烧杯中的混合物温度都升高到30℃,所得溶液溶质质量分数的大小关系是
甲=乙>丙
甲=乙>丙
.
(5)现要配制20℃时70g10%的甲溶液.该实验的部分操作如图2所示.
①需要称取甲的质量是
7g
7g
,称量时图A出现了右盘低的现象,接下来的操作应该是
D
D
.
A.左边的平衡螺丝向左调 B.将游码向左移动
C.右盘中减少砝码 D.左盘中增加甲
②量取水时,如果按照图B的方法读数,会使配制的溶液溶质质量分数
偏小
偏小
(填“偏大”或“偏小”).
③图C中用玻璃棒搅拌的作用是
搅拌、加速固体溶解
搅拌、加速固体溶解
.
(6)下列选项为配制甲溶液的步骤,其先后顺序正确的是
B
B
A.称量-计算-量取-溶解-转液贴签
B.计算-称量-量取-溶解-转液贴签
C.计算-称量-量取-转液贴签-溶解
D.计算-溶解-称量-转液贴签-量取.

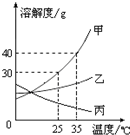 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
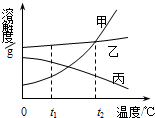 甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法中不正确的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法中不正确的是( )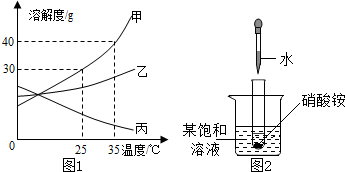 甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答: