
题目列表(包括答案和解析)

| 实验方案 | 实验现象 | 有关化学方程式 | 实验结论 |
| ①取样,先向溶液中滴加过量的 CaCl2或BaCl2或Ca(NO3)2或Ba(NO3)2 CaCl2或BaCl2或Ca(NO3)2或Ba(NO3)2 溶液; |
产生白色沉淀 | CaCl2+Na2CO3═CaCO3↓+2NaCl CaCl2+Na2CO3═CaCO3↓+2NaCl |
D溶液中有NaOH剩余. |
| ②静置,取上层清液,滴加 FeCl3或Fe(NO3)3 FeCl3或Fe(NO3)3 溶液. |
产生红褐色沉淀 | 3NaOH+FeCl3═Fe(OH)3↓+3NaCl 3NaOH+FeCl3═Fe(OH)3↓+3NaCl |
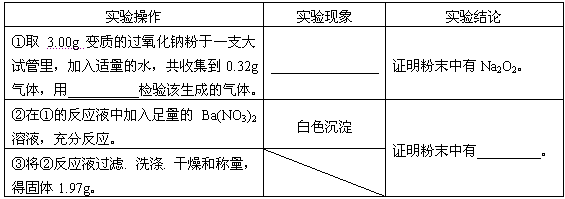
| 实验操作 | 实验现象 | 实验结论 |
| ①取3.00g变质的过氧化钠粉于一支大试管里,加入适量的水,共收集到0.32g气体,用______检验该生成的气体. | _______________. | 证明粉末中有Na2O2. |
| ②在①的反应液中加入足量的Ba(NO3)2溶液,充分反应. | 白色沉淀 | 证明粉末中有_____. |
| ③将②反应液过滤、洗涤、干燥和称量,得固体1.97g. | \ |
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量变质的过氧化钠粉末一支试管里,加入过量的水,然后用______检验该生成的气体. | ______ | 证明粉末中有Na2O2. |
| ②在①的剩余的溶液中加入足量的硝酸钡溶液,充分反应. | 产生白色沉淀 | 证明粉末中有______. |
| ③在①的剩余的溶液中加入足量的硫酸铜溶液. | ______ |
| 实验操作 | 实验现象 | 实验结论 |
| ①取3.00g变质的过氧化钠粉于一支大试管里,加入适量的水,共收集到0.32g气体,用______检验该生成的气体. | _______________. | 证明粉末中有Na2O2. |
| ②在①的反应液中加入足量的Ba(NO3)2溶液,充分反应. | 白色沉淀 | 证明粉末中有_____. |
| ③将②反应液过滤、洗涤、干燥和称量,得固体1.97g. | \ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com