
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)

дкРЯЪІЕФжИЕМЯТЃЌЭЌбЇУЧНјааСЫгаШЄЕФЛЏбЇЪЕбщЬНОПЃК
вЛЁЂВтЖЈПеЦјжабѕЦјКЌСП
ЭМ1ЫљЪОЕФЪЧаЁССЭЌбЇгУКьСздкПеЦјжаШМЩеЕФВтЖЈЗНЗЈЃЎЙ§ГЬЪЧЃК
Ек1ВНЃКНЋМЏЦјЦПШнЛ§ЛЎЗжЮЊЮхЕШЗнЃЌВЂзіКУБъМЧЃЎ
Ек2ВНЃКЕуШМШМЩеГзФкЕФКьСзЃЌЩьШыМЏЦјЦПжаВЂАбШћзгШћНєЁЃ
Ек3ВНЃКД§КьСзЯЈУ№ВЂРфШДКѓЃЌДђПЊЕЏЛЩМаЃЌЗЂЯжЫЎБЛЮќШыМЏЦјЦПжаЃЌНјШыМЏЦјЦПжаЫЎЕФЬхЛ§дМЮЊМЏЦјЦПзмШнЛ§ЕФ1/5ЃЎЧыЛиД№ЯТСаЮЪЬтЃК

ЂйЕк2ВНКьСзШМЩеЪБЕФЯжЯѓ ЃЌ
ЛЏбЇЗДгІБэДяЪНЃК ЁЃ
ЂкЪЕбщЭъБЯЃЌШєНјШыМЏЦјЦПжаЫЎЕФЬхЛ§ВЛЕНзмШнЛ§ЕФ1/5ЃЌ
ФуШЯЮЊЕМжТетвЛНсЙћЕФдвђПЩФмЪЧ ЁЃ
AЁЂМЏЦјЦПЕзВПЕФЫЎеМСЫвЛВПЗжЬхЛ§
BЁЂКьСзЙ§Щй
CЁЂКьСзУЛгаШМЩеЭъОЭМБзХДђПЊСЫжЙЫЎМа
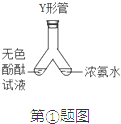
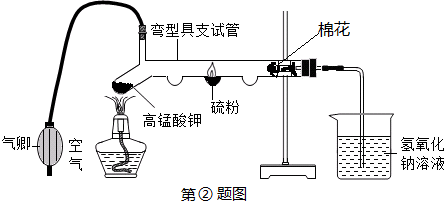
ЂлаЁВЉЭЌбЇЖдЪЕбщНјааЗДЫМКѓЃЌЬсГіСЫИФНјЗНЗЈЃЈШчЭМ2ЫљЪОЃЉЃЌаЁВЉдке§ЪНПЊЪМЪЕбщЧАЃЌМаНєЕЏЛЩМаЃЌНЋзЂЩфЦїЛюШћДг20mLПЬЖШДІЭЦжС15mLДІЃЌШЛКѓЫЩПЊЛюШћЃЌЙлВьЕНЛюШћЗЕЛижС20mLПЬЖШДІЃЎИУВйзїЕФжївЊФПЕФЪЧ ЃЌФуШЯЮЊИФНјКѓЕФгХЕуЪЧ ЁЃ
ЖўЁЂаЁгрдФЖСПЮЭтзЪСЯЕУжЊЃКЫЋбѕЫЎЗжНтГ§СЫгУЖўбѕЛЏУЬЃЈMnO2ЃЉЛЙПЩгУбѕЛЏЭЃЈCuOЃЉЕШЮяжЪзїДпЛЏМСЃЌгкЪЧЫћЖдбѕЛЏЭВњЩњСЫЬНОПаЫШЄЁЃ
ЁОЬсГіЮЪЬтЁПбѕЛЏЭЪЧЗёвВФмзїТШЫсМиЗжНтЕФДпЛЏМСЃПЫќЪЧЗёБШЖўбѕЛЏУЬДпЛЏаЇЙћИќКУЃП
ЁОЩшМЦЪЕбщЁПаЁгрвдЩњГЩЕШЬхЛ§ЕФбѕЦјЮЊБъзМЃЌЩшМЦСЫЯТСаШ§зщЪЕбщЃЈЦфЫќПЩФмгАЯьЪЕбщ
ЕФвђЫиОљКіТдЃЉ
| ЪЕбщађКХ | ТШЫсМижЪСП | ЦфЫћЮяжЪжЪСП | Д§ВтЪ§Он |
| Ђй | 1.2g | / | |
| Ђк | 1.2g | CuO 0.5g | |
| Ђл | 1.2g | MnO2 0.5g | |
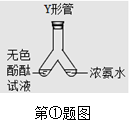

дкРЯЪІЕФжИЕМЯТЃЌЭЌбЇУЧНјааСЫгаШЄЕФЛЏбЇЪЕбщЬНОПЃК
вЛЁЂВтЖЈПеЦјжабѕЦјКЌСП
ЭМ1ЫљЪОЕФЪЧаЁССЭЌбЇгУКьСздкПеЦјжаШМЩеЕФВтЖЈЗНЗЈЃЎЙ§ГЬЪЧЃК
Ек1ВНЃКНЋМЏЦјЦПШнЛ§ЛЎЗжЮЊЮхЕШЗнЃЌВЂзіКУБъМЧЃЎ
Ек2ВНЃКЕуШМШМЩеГзФкЕФКьСзЃЌЩьШыМЏЦјЦПжаВЂАбШћзгШћНєЁЃ
Ек3ВНЃКД§КьСзЯЈУ№ВЂРфШДКѓЃЌДђПЊЕЏЛЩМаЃЌЗЂЯжЫЎБЛЮќШыМЏЦјЦПжаЃЌНјШыМЏЦјЦПжаЫЎЕФЬхЛ§дМЮЊМЏЦјЦПзмШнЛ§ЕФ1/5ЃЎЧыЛиД№ЯТСаЮЪЬтЃК


ЂйЕк2ВНКьСзШМЩеЪБЕФЯжЯѓ ЃЌ
ЛЏбЇЗДгІБэДяЪНЃК ЁЃ
ЂкЪЕбщЭъБЯЃЌШєНјШыМЏЦјЦПжаЫЎЕФЬхЛ§ВЛЕНзмШнЛ§ЕФ1/5ЃЌ
ФуШЯЮЊЕМжТетвЛНсЙћЕФдвђПЩФмЪЧ ЁЃ
AЁЂМЏЦјЦПЕзВПЕФЫЎеМСЫвЛВПЗжЬхЛ§
BЁЂКьСзЙ§Щй
CЁЂКьСзУЛгаШМЩеЭъОЭМБзХДђПЊСЫжЙЫЎМа
ЂлаЁВЉЭЌбЇЖдЪЕбщНјааЗДЫМКѓЃЌЬсГіСЫИФНјЗНЗЈЃЈШчЭМ2ЫљЪОЃЉЃЌаЁВЉдке§ЪНПЊЪМЪЕбщЧАЃЌМаНєЕЏЛЩМаЃЌНЋзЂЩфЦїЛюШћДг20mLПЬЖШДІЭЦжС15mLДІЃЌШЛКѓЫЩПЊЛюШћЃЌЙлВьЕНЛюШћЗЕЛижС20mLПЬЖШДІЃЎИУВйзїЕФжївЊФПЕФЪЧ ЃЌФуШЯЮЊИФНјКѓЕФгХЕуЪЧ ЁЃ
ЖўЁЂаЁгрдФЖСПЮЭтзЪСЯЕУжЊЃКЫЋбѕЫЎЗжНтГ§СЫгУЖўбѕЛЏУЬЃЈMnO2ЃЉЛЙПЩгУбѕЛЏЭЃЈCuOЃЉЕШЮяжЪзїДпЛЏМСЃЌгкЪЧЫћЖдбѕЛЏЭВњЩњСЫЬНОПаЫШЄЁЃ
ЁОЬсГіЮЪЬтЁПбѕЛЏЭЪЧЗёвВФмзїТШЫсМиЗжНтЕФДпЛЏМСЃПЫќЪЧЗёБШЖўбѕЛЏУЬДпЛЏаЇЙћИќКУЃП
ЁОЩшМЦЪЕбщЁПаЁгрвдЩњГЩЕШЬхЛ§ЕФбѕЦјЮЊБъзМЃЌЩшМЦСЫЯТСаШ§зщЪЕбщЃЈЦфЫќПЩФмгАЯьЪЕбщ
ЕФвђЫиОљКіТдЃЉ
|
ЪЕбщађКХ |
ТШЫсМижЪСП |
ЦфЫћЮяжЪжЪСП |
Д§ВтЪ§Он |
|
Ђй |
1.2g |
/ |
|
|
Ђк |
1.2g |
CuO 0.5g |
|
|
Ђл |
1.2g |
MnO2 0.5g |
|
ЂйЩЯЪіЪЕбщгІВтСПЕФЁАД§ВтЪ§ОнЁБЪЧ ЁЃ
ЂкШєЪЕбщЂкБШЪЕбщЂйЕФЁАД§ВтЪ§ОнЁБИќ (ЬюЁАДѓЁБЛђЁАаЁЁБ)ЃЌЫЕУїбѕЛЏЭФмМгПьТШЫсМиЕФЗжНтЁЃ
ЂлНЋЪЕбщЂкЗДгІЪЃгрЕФЙЬЬхШЁГіКѓОЯДЕгЁЂИЩдяЃЌдйДЮОЋШЗГЦСПЕУЕН0.5gКкЩЋЗлФЉЃЌетбљзіЕФФПЕФЪЧ ЃЌаЁгрЭЌбЇШЯЮЊбѕЛЏЭПЯЖЈЪЧТШЫсМиЗжНтЕФДпЛЏМСЃЌЕЋаЁДОЭЌбЇЖдДЫЬсГіСЫвьвщЃЌаЁДОЭЌбЇЩшМЦСЫШчЯТЪЕбщЃК
НЋЕкЖўДЮОЋШЗГЦСПЕУЕНЕФ0.5gКкЩЋЗлФЉКЭ1.2gТШЫсМиЛьКЯЗХШыЪдЙмжаЃЌМгШШЃЌЩьШыДјЛ№аЧФОЬѕЃЌЗЂЯжФОЬѕКмПьИДШМЁЃ
аЁДОЭЌбЇетбљзіФПЕФЪЧ ЃЌ
ЁОдЄЦкНсТлЁПбѕЛЏЭвВФмзїТШЫсМиЕФДпЛЏМСЁЃ
ЁОЦРМлЩшМЦЁПФуШЯЮЊаЁгрЩшМЦЪЕбщЂлКЭЪЕбщЂкЖдБШЕФФПЕФЪЧ ЃЛаДГіЪЕбщЂкЗДгІЕФБэДяЪН ЁЃ
Ш§ЁЂгаШЄЕФИФНјЪЕбщ
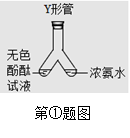
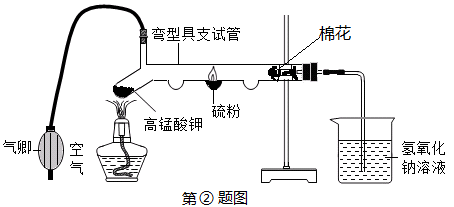
ЂйаЁЧчЭЌбЇбЇСЫЗжзгаджЪетНкФкШнКѓЃЌИФНјСЫЪщБОЩЯЬНОПЗжзгдЫЖЏЕФЪЕбщЁЃаЁЧчЭЌбЇевРДЗЯЦњЕФвНСЦгУЦЗ-----ЮЂаЭY аЮЙмЃЌЩшМЦШчЭМ1ЫљЪОЪЕбщЃЌЫ§НјааИУЪЕбщЪЧЮЊСЫЬНОП ЃЌЪЕбщЙ§ГЬжаФмПДЕНЕФЯжЯѓЪЧ ЃЌаЁЧчЭЌбЇЩшМЦЕФЪЕбщгХЕуЪЧ ЁЃ

ЂкРћгУШчЭМзАжУНјааЁАСђШМЩеЁБЕФЪЕбщЃКгУЦјЧфЃЈФмВЛЖЯЙФШыПеЦјЕФзАжУЃЉВЛЖЯЕиЯђЭфаЭОпжЇЪдЙмжаЙФШыПеЦјЃЌЭЌЪБгУОЦОЋЕЦИјСђЗлМгШШжСШМЩеЃЌвЦШЅОЦОЋЕЦЃЌПЩЙлВьЕНЮЂШѕЕФЕРЖЩЋЛ№бцЃЛШЛКѓЭЃжЙЙФШыПеЦјЃЌдйгУОЦОЋЕЦИјИпУЬЫсМиМгШШЃЌЪЙСђдкДПбѕжаМЬајШМЩеЃЌЙлВьЕНЁЁ ЁЁЛ№бцЁЃ
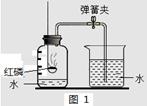
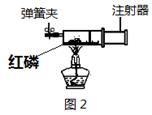
аДГіЪЕбщжаСђЛЧШМЩеЕФЛЏбЇЗДгІБэДяЪНЃК ЃЌИУЪЕбщзАжУЕФжївЊгХЕуЪЧдкЯћГ§гаКІЦјЬхЖдЛЗОГЮлШОЕФЧАЬсЯТгаРћгкЁЁ ЁЁЃЎФуЭЦЖЯЩеБжаЕФЧтбѕЛЏФЦШмвКЕФ зїгУЪЧ ЁЃ

| ЪЕбщађКХ | ТШЫсМижЪСП | ЦфЫћЮяжЪжЪСП | Д§ВтЪ§Он |
| Ђй | 1.2g | / | |
| Ђк | 1.2g | CuO 0.5g | |
| Ђл | 1.2g | MnO2 0.5g | |
| 1 |
| 5 |

| ЪЕбщађКХ | ТШЫсМижЪСП | ЦфЫћЮяжЪжЪСП | Д§ВтЪ§Он |
| Ђй | 1.2g | / | |
| Ђк | 1.2g | CuO 0.5g | |
| Ђл | 1.2g | MnO2 0.5g |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com