
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
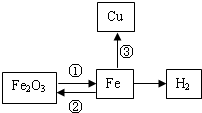 ππΩ®÷™ ∂Õ¯¬Á «“ª÷÷÷ÿ“™µƒ—ßœ∞∑Ω∑®£ÆÕºŒ™ƒ≥–£ªØ—ß—ßœ∞–°◊ȵƒ–°—ÙÕ¨—ߪÊ÷∆µƒÃ˙µƒªØ—ß–‘÷ Õ¯¬Á æ“‚Õº£Æ«Î∑÷Œˆªÿ¥œ¬¡–Œ £∫
ππΩ®÷™ ∂Õ¯¬Á «“ª÷÷÷ÿ“™µƒ—ßœ∞∑Ω∑®£ÆÕºŒ™ƒ≥–£ªØ—ß—ßœ∞–°◊ȵƒ–°—ÙÕ¨—ߪÊ÷∆µƒÃ˙µƒªØ—ß–‘÷ Õ¯¬Á æ“‚Õº£Æ«Î∑÷Œˆªÿ¥œ¬¡–Œ £∫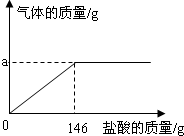
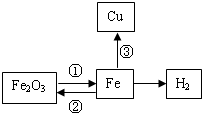 ππΩ®÷™ ∂Õ¯¬Á «“ª÷÷÷ÿ“™µƒ—ßœ∞∑Ω∑®£ÆÕºŒ™ƒ≥–£ªØ—ß—ßœ∞–°◊ȵƒ–°—ÙÕ¨—ߪÊ÷∆µƒÃ˙µƒªØ—ß–‘÷ Õ¯¬Á æ“‚Õº£Æ«Î∑÷Œˆªÿ¥œ¬¡–Œ £∫
ππΩ®÷™ ∂Õ¯¬Á «“ª÷÷÷ÿ“™µƒ—ßœ∞∑Ω∑®£ÆÕºŒ™ƒ≥–£ªØ—ß—ßœ∞–°◊ȵƒ–°—ÙÕ¨—ߪÊ÷∆µƒÃ˙µƒªØ—ß–‘÷ Õ¯¬Á æ“‚Õº£Æ«Î∑÷Œˆªÿ¥œ¬¡–Œ £∫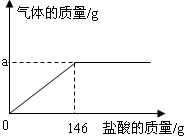
| ||
| ||
£®√øø’2∑÷£¨π≤14∑÷£©«‚ªØ∏∆£®CaH2£©πÃà«“ª÷÷¥¢«‚≤ƒ¡œ£¨ «µ«…Ω‘À∂Ø‘±≥£”√µƒƒÐ‘¥Ã·π©º¡°£ƒ≥ªØ—ß–°◊ȵƒÕ¨—ß‘⁄¿œ ¶µƒ÷∏µºœ¬÷∆±∏«‚ªØ∏∆°£
°æ≤È‘ƒ◊ ¡œ°ø
«‚ªØ∏∆Õ®≥£”√«‚∆¯”Î∏∆º”»»÷∆µ√°£
«‚ªØ∏∆“™√Ð∑‚±£¥Ê£¨”ˆÀÆ∑¥”¶…˙≥…«‚—ıªØ∏∆∫Õ«‚∆¯°£
∏∆”ˆÀÆ¡¢º¥∑¢…˙æÁ¡“∑¥”¶…˙≥…«‚—ıªØ∏∆∫Õ«‚∆¯£¨≤¢∑≈≥ˆ¥Û¡øµƒ»»°£
±Í◊º◊¥øˆœ¬«‚∆¯µƒ√Ð∂»Œ™0.09g/L°£
°æΩ¯–– µ—È°ø
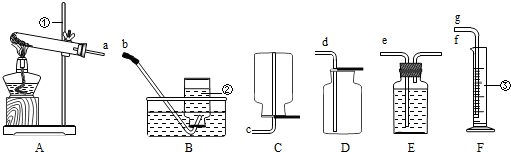
–°◊ÈÕ¨—߅˺∆µƒ÷∆»°◊∞÷√»Áœ¬ÕºÀ˘ 森πÃ∂®◊∞÷√¬‘£©°£
ªÿ¥œ¬¡–Œ £∫
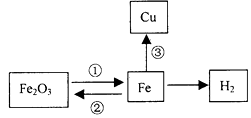
£®1£©–¥≥ˆA÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã Ω °£
£®2£©B°¢D÷–À˘ ¢ ‘º¡œýÕ¨£¨∏√ ‘º¡Œ™ £¨∆‰◊˜”√∑÷± « °¢ °£
£®3£© µ—È ±œ»¥Úø™A÷–ªÓ»˚£¨“ª∂Œ ±º‰∫Û£¨‘Ÿµ„»ºC÷–æ∆æ´µ∆£¨∆‰ƒøµƒ «
°£
£®4£©◊∞÷√C÷–÷∆»°«‚ªØ∏∆µƒªØ—ß∑Ω≥Ã Ω « °£
°æ µ—È∑¥Àº°ø–°◊ÈÕ¨—ßÕ®π˝∑¥ÀºÃ·≥ˆŒ £∫…œ ˆ÷∆µ√µƒ«‚ªØ∏∆ «∑Ò¥ø檣ø
°æ—˘∆∑≥…∑÷µƒ≤¬œÎ°øÕ®π˝…œ ˆ∑Ω∑®÷∆µ√µƒ«‚ªØ∏∆—˘∆∑µƒ≥…∑÷”–œ¬¡–¡Ω÷÷≤¬œÎ£∫
À˚√«∞¥’’œ¬ÕºÀ˘ æ◊∞÷√Ω¯––ºÏ—È°£
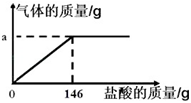
°æ…˺∆ µ—È°ø»ÙÀ˘º”»Îµƒ«‚ªØ∏∆—˘∆∑÷ ¡øŒ™2.1 g£¨«Î—È÷§∏√«‚ªØ∏∆—˘∆∑ «∑Ò¥ø檣ø
£®“™«Û≤Ÿ◊˜°¢ ˝æð∫ÕΩ·¬€£©°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com