
题目列表(包括答案和解析)
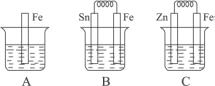
(1)A中反应的离子方程式为__________________________________________________。
(2)B中Sn极的电极反应为___________,Sn极附近溶液的pH(填“增大”“减小”或“不变”)___________。
(3)C中被腐蚀的金属是___________,总反应为___________________________________。
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是__________(用A、B、C填空)。
(1)反应开始时生成N2O4的速率v(A)____________v(B)。
(2)反应中生成N2O4的速率v(A) ____________v(B)。
(3)平衡时两容器中分子总数n(A) ____________n(B)。
(4)达到平衡时两容器压强p(A) ____________p(B)。
请回答下列问题。
(1)Z的原子结构示意图为___________;化合物BA4的电子式为___________。
(2)化合物Y2X2中含有的化学键类型有___________(填序号)。
A.离子键 B.极性共价键
C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是_____________________(填化学式),其主要原因是_____________________________。
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为________________________。
(5)常温常压下,由A、B、X可组成的液态物质甲。现有2.
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42— 、OH- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
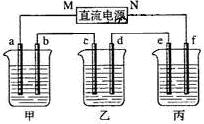
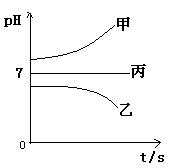
接通电源,经过一段时间后,测得乙中c电极质量增加了16g。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”)
电极b上发生的电极反应为 ;
(2)计算电极e上生成的气体在标准状态下的体积: ;
(3)写出乙烧杯的电解池反应
(4)若经过一段时间后,测得乙中c电极质量增加了16g,要使丙恢复到原来的状态,操作是
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。
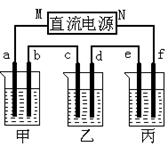
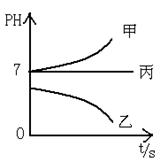
接通电源,经过一端时间后,测得乙中C电极质量增加了27克。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的_______极(填写“正”或“负”),甲、乙电解质分别为_______、_______(填写化学式)。
(2)计算电极f上生成的气体在标准状况下的体积:_____________。
(3)写出乙烧杯的电解池反应_____________________________。
(4)若电解后甲溶液![]() 的体积为25L,则该溶液的pH为___________ 。
的体积为25L,则该溶液的pH为___________ 。
(5)要使丙恢复到原来的状态,应加入_____ __ g 。(填写化学式)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com