
题目列表(包括答案和解析)

金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
【实验目的】测定金属铁、铜和镁的活动性强弱
【所用试剂】稀硫酸、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】步骤Ⅰ 将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ 将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ 将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中。
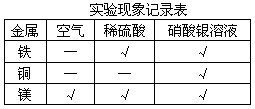
实验现象记录表
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 铁 | - | | |
| 铜 | - | - | |
| 镁 | | | |
金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能![]() 优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
【实验目的】 测定金属铁、铜和镁的活动性强弱
【所用试剂】 稀硫酸、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】
步骤Ⅰ 将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ 将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ 将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中。[来源:学科网]
【实验记录】用“√”表示能观察到实验现象,用“—”表示观察不到实验现象(见右表)。
⑴通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是
⑵运用“控制变量法”设计实验方案是化学研究的重要方法。步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是 。写出镁和稀硫酸反应的化学方程式 ,此反应属于 。
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是 (用元素符号表示)
【反思交流】 若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是 。
金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
【实验目的】测定金属铁、铜和镁的活动性强弱
【所用试剂】稀硫酸、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】步骤Ⅰ 将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ 将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ 将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中。
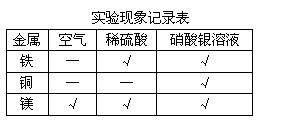
实验现象记录表
金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
铁 | - |
|
|
铜 | - | - |
|
镁 |
|
|
|
【实验记录】用“”表示能观察到实验现象,用“-”表示观察不到实验现象(见表)。
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是????????????????????????? 。
(2)运用“控制变量法”设计实验方案是化学研究的重要方法。步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是??????????????????????????? 。写出镁和稀硫酸反应的化学方程式????????????????????????????????? ,此反应属于????????? 。
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是???????????? (用元素符号表示)。
【反思交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是??????????????????????? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com