
题目列表(包括答案和解析)

回答下列问题:
(1)X分子中含________键(填“极性”或“非极性”),X为__________分子(同前)。
(2)在上述转化过程中,作还原剂的物质有(填物质的化学式)__________。
(3)A与硝酸反应的化学方程式为________________________________________________。
(4)测定气体C的相对分子质量时,测得的数值与气体C的相对分子质量有差异的原因是(用化学方程式表示)_________________________________________________________。

| ||
| ||
| ||
| ||
| ||
| △ |
| ||
| △ |
 Ⅰ
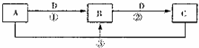
Ⅰ(13分)A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空:

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是 ;工业上制取A的离子方程式为 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
(3)若D是氯碱工业的主要产品,B有两性,则反应②的离子方程式是 。
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式 。
(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
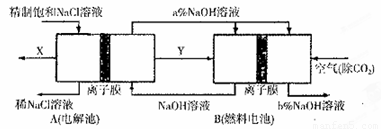
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a% b%(填“>”、“=”或“<”)
②写出燃料电池B中负极上发生的电极反应 。
 Ⅰ
Ⅰ湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com