
题目列表(包括答案和解析)
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,a的分子式是_____,b的结构式是_______;中心原子的杂化轨道类型分别是________、_________;a分子的立体结构是____________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体;
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式) ;
(4)Y与Z比较,电负性较大的是____________;
(5)W的元素符号是 ,其+2价离子的核外电子排布式是
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,a的分子式是_____,b的结构式是_______;中心原子的杂化轨道类型分别是________、_________;a分子的立体结构是____________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体;
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式) ;
(4)Y与Z比较,电负性较大的是____________;
(5)W的元素符号是 ,其+2价离子的核外电子排布式是




| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
| ||
| ||


X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少、构成蛋白质的重要组成元素;Z的基态原子核外9个轨道上填充了电子,且核外有2个未成对电子,与Y不同族;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1) 常温常压下Z单质是_______晶体(填类型),微粒间通过______形成晶体(填微粒间相互作用的类型)。Y2分子中存在![]() 键和
键和![]() 键个数之比为____________。
键个数之比为____________。
(2) X-H和Y—H属于极性共价键,其中极性较强的键是______(X、Y用元素符号表示)。X的第一电离能比Y的______(填“大”或“小“)。
(3) 写出X单质与Z的最高价氧化物对应的水化物的浓溶液反应的化学方程式____________________________________________________________
(4) W的基态原子的外围电子排布式是____________。
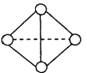
(5) 已知一种分子Y4分子结构如上图所示:断裂1molY—Y吸收167KJ的热量,生成1molY![]() Y放出942KJ热量。试写出由Y4气态分子变成Y2气态分子的热化学方程式________________________
Y放出942KJ热量。试写出由Y4气态分子变成Y2气态分子的热化学方程式________________________
(10分) 科学家用NaNO3和Na2O在一定条件下等物质的量化合制得晶体A,A由钠离子和某阴离子B构成, 则:
(1)A的化学式为 , A 与Na3PO4比较,其稳定性A Na3PO4(填“>”或“<”),阴离子B的空间结构最有可能是 (填序号);
①直线型 ②平面三角形 ③三角锥形 ④正四面体
(2)A对CO2特别敏感,与CO2反应相当剧烈,生成两种常见的物质,该反应的化学方程式为: ;
(3)此外,科学家还制备了另一种钠盐D,其与A的组成元素完全相同,D中的阴离子与A中的阴离子表观形式相同(元素种类和原子个数均相同),但D中阴离子的结构中含有一个过氧键:-O-O- ,电导实验表明,同条件下其电导能力与NaCl相同,该阴离子的化学式为 ,其与水反应生成过氧化氢的离子方程式为 ,该反应 (填“是”或“不是”)氧化-还原反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com