
题目列表(包括答案和解析)
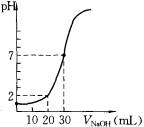
(14分)用一定物质的量浓度的NaOH溶液滴定10.00 mL已知浓度的盐酸,滴定结果如图所示。回答下列问题:
(1)有关滴定的操作可分解为如下几步,并补充完整。①用NaOH溶液润洗滴定管。②取NaOH溶液注入碱式滴定管至“0”刻度以上2~3 mL。③ ④调节液面至“0”或“0”刻度以下,记下读数。⑤移取10.00 mL盐酸注入锥形瓶中,加入酚酞。⑥把锥形瓶放在滴定管的下面,用氢氧化钠溶液滴定并记下读数。
(2)若滴定前俯视滴定管读数,滴定后平视刻度读数,则会使氢氧化钠浓度的测定结果 (填“偏高”“偏低”或“不变”)。
(3)如用酚酞作指示剂,则滴定终点的实验现象是 。
(4)c(HCl)= mol·L-1
(5)c(NaOH) = mol·L-1
(6)右图表示50 mL滴定管中液面的位置,如果液面处的读数是a ,则滴定管中液体的体积(填代号) 。
| A.是a mL | B.是(50-a)mL |
| C.一定大于a mL | D.一定大于(50-a)mL |
(14分)用一定物质的量浓度的NaOH溶液滴定10.00 mL已知浓度的盐酸,滴定结果如图所示。回答下列问题:

(1)有关滴定的操作可分解为如下几步,并补充完整。①用NaOH溶液润洗滴定管。②取NaOH溶液注入碱式滴定管至“0”刻度以上2~3 mL。③ ④调节液面至“0”或“0”刻度以下,记下读数。⑤移取10.00 mL盐酸注入锥形瓶中,加入酚酞。⑥把锥形瓶放在滴定管的下面,用氢氧化钠溶液滴定并记下读数。
(2)若滴定前俯视滴定管读数,滴定后平视刻度读数,则会使氢氧化钠浓度的测定结果 (填“偏高”“偏低”或“不变”)。

(3)如用酚酞作指示剂,则滴定终点的实验现象是 。
(4)c(HCl)= mol·L-1
(5)c(NaOH) = mol·L-1
(6)右图表示50 mL滴定管中液面的位置,如果液面处的读数是a ,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(50-a)mL
C.一定大于a mL D.一定大于(50-a)mL
(7)常温下,用0.01 mol•L-1H2SO4溶液滴定0.01 mol•L-1 NaOH溶液,中和后加水至100 ml。若滴定到终点时少加一滴H2SO4(设1滴为0.05 ml)。则此时溶液的pH为 。
| A.是a mL | B.是(50-a)mL |
| C.一定大于a mL | D.一定大于(50-a)mL |
(1)在(Ⅰ)的情况下,溶质为(写化学式)____________,其物质的量之比是____________,标准状况下CO2气体的体积为____________。
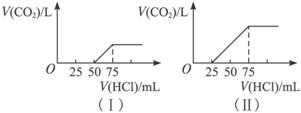
(2)在(Ⅱ)情况下,溶质为(写化学式)____________,其物质的量之比是____________,标准状况下CO2气体的体积为____________。
(3)求原NaOH溶液的物质的量浓度。
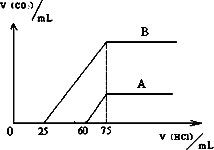
取等物质的量浓度的NaOH溶液两份A和B,每份50 mL,向其中各通入一定量的CO2,然后各取溶液10 mL,分别将其稀释为100 mL,分别向稀释后的溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生CO2气体体积与所加盐酸体积之间的关系如下图所示.
试回答下列问题:
(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式)________,其物质的量之比为________;加盐酸后产生CO2体积的最大值为________mL(不考虑CO2的溶解,下同).
(2)曲线B表明,原溶液中通入CO2后,所得溶液中的溶质为(写化学式)________,其物质的量之比为________;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com