
题目列表(包括答案和解析)
 nC(气)+2D(气),5分钟时反应达平衡状态,生成1摩D; 经测定,以C表示的平均反应速度为0.1摩/(升?分),下列结论中错误的是
nC(气)+2D(气),5分钟时反应达平衡状态,生成1摩D; 经测定,以C表示的平均反应速度为0.1摩/(升?分),下列结论中错误的是
| A.①、② | B.①、④ | C.②、③ | D.③、④ |
 nC(气)+2D(气),5分钟时反应达平衡状态,生成1摩D; 经测定,以C表示的平均反应速度为0.1摩/,下列结论中错误的是
nC(气)+2D(气),5分钟时反应达平衡状态,生成1摩D; 经测定,以C表示的平均反应速度为0.1摩/,下列结论中错误的是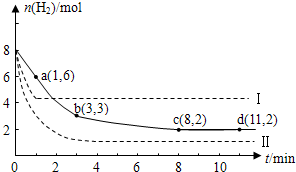 (2011?闵行区二模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
(2011?闵行区二模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com