
题目列表(包括答案和解析)
物质 | A | B | CO | H2 |
燃烧热/kJ·mol-1 | 725 | 5 518 | 283 | 286 |
A、B按不同比例混合的燃料有91.2 g,在足量的O2中燃烧时,放出的热量Q与B的物质的量分数x的关系如下图所示。
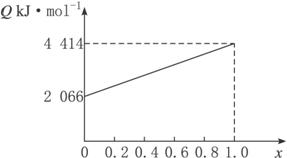
(1)求A、B的相对分子质量。
(2)等物质的量A、B混合的燃料有73 g,在160 L O2中完全燃烧,得到104 L气体,通过碱石灰吸收后剩余3.2 L(气体体积均在标准状况下测定)。由此可推得混合物中原子个数比N(C)∶N(H)∶N(O)是多少?写出A和B的化学式。
(3)求1 mol由A、B等物质的量混合而成的燃料在一定的氧气中燃烧,放出2 980 kJ的热量,则反应中生成CO的物质的量。
下列说法正确的是
A.同温同压下,H2(g)+Cl2(g)==2HCl(g)在光照和点燃条件下的△H相同
B.铅蓄电池放电时的负极和充电时的阴极均发生还原反应
C.已知:H2(g) + I2(g)2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
D.已知在101 kPa时,2 g碳燃烧生成CO放出热量为Q kJ,则碳的燃烧热为6Q kJ·mol-1
【解析】反应热与反应条件无关,A正确。铅蓄电池放电时的正极和充电时的阴极均发生还原反应,B错误。选项C中是可逆反应,所以254g I2(g)和2gH2(g)充分反应放出的热量小于9.48 kJ,C不正确。燃烧热是指在一定条件下,1mol物质完全燃烧生成稳定的氧化物时所放出的能量,因此D不正确。答案是A。
下列说法正确的是
A.同温同压下,H2(g)+Cl2(g)==2HCl(g)在光照和点燃条件下的△H相同
B.铅蓄电池放电时的负极和充电时的阴极均发生还原反应
C.已知:H2(g) + I2(g) 2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
2HI(g);△H =-9.48 kJ/mol,若将254g I2(g)和2gH2(g)充分反应可放出9.48 kJ的热量
D.已知在101 kPa时,2 g碳燃烧生成CO放出热量为Q kJ,则碳的燃烧热为6Q kJ·mol-1
【解析】反应热与反应条件无关,A正确。铅蓄电池放电时的正极和充电时的阴极均发生还原反应,B错误。选项C中是可逆反应,所以254g I2(g)和2gH2(g)充分反应放出的热量小于9.48 kJ,C不正确。燃烧热是指在一定条件下,1mol物质完全燃烧生成稳定的氧化物时所放出的能量,因此D不正确。答案是A。
| A、1 | B、2 | C、3 | D、4 |
| A、3 | B、4 | C、5 | D、6 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com