
A、B、C、D分别是HNO
3、Ba(NO
3)
2、NH
4Cl、NaOH四种溶液中的一种.现利用另一种常见溶液X,用下图所示的方法,可将它们一一确定.请回答以下问题:
(1)B的化学式是
Ba(NO3)2
Ba(NO3)2
A的电子式为
(2)写出在X溶液中加入过量NH
3?H
2O的离子反应方程式
Cu2++4NH3?H2O=Cu(NH3)42++4H2O
Cu2++4NH3?H2O=Cu(NH3)42++4H2O
.
(3)有学生分别用其他试剂来鉴别上述四种溶液:
①用物质Y一次性鉴别上述四种物质,结果发现第一种溶液中反应后溶液呈黄色,第二种溶液中有白色沉淀产生,第三种溶液中有能使湿润的红色石蕊试纸变蓝的气体产生,则Y是
(NH4)2Fe(SO4)2
(NH4)2Fe(SO4)2
(用化学式表示).Y溶液与稀硝酸反应的离子方程式为
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
.
②若用明矾鉴别上述四种物质,写出能检验出NH
4Cl溶液所涉及的所有离子反应方程式:Ba
2++SO
42-=BaSO
4↓、
Al3++4OH-=AlO2-+2H2O
Al3++4OH-=AlO2-+2H2O
.
③有学生用MgSO
4来鉴别上述四种溶液,在生成的白色沉淀Mg(OH)
2中分别加入HNO
3和NH
4Cl溶液,发现沉淀均溶解.有以下两种解释,同时提供下表数据:
A.NH
4Cl溶液能使Mg(OH)
2溶解,主要是NH
4+水解产生H
+的缘故.
B.NH
4Cl溶液能使Mg(OH)
2溶解,主要是NH
4+结合OH
-的缘故.
| 电解质 |
HF |
HCOOH |
CH3COOH |
HCN |
NH3?H2O |
| 电离度 |
8.00% |
7.16% |
1.32% |
0.01% |
1.33% |
能证明A和B哪一种解释正确,可以在生成的Mg(OH)
2沉淀中加入一种物质,这种物质是
CH3COONH4
CH3COONH4
(用化学式表示).

 A、B、C、D分别是HNO3、Ba(NO3)2、NH4Cl、NaOH四种溶液中的一种.现利用另一种常见溶液X,用下图所示的方法,可将它们一一确定.请回答以下问题:
A、B、C、D分别是HNO3、Ba(NO3)2、NH4Cl、NaOH四种溶液中的一种.现利用另一种常见溶液X,用下图所示的方法,可将它们一一确定.请回答以下问题:

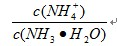 的值
的值