某学生取纯净的Na
2SO
3?7H
2O 50.00g,在密闭容器中经600
0C以上的强热至恒重,分析及计算表明,恒重后的样品质量相当于无水亚硫酸钠的计算值,而且各元素的组成也符合计算值,但将它溶于水,却发现溶液的碱性大大高于同时配制的亚硫酸钠溶液.经过他的实验和思考,这位同学解释了这种反常现象.
(1)他将恒重后的样品溶于水配成溶液,为加速溶解,可采取
搅拌或加热
搅拌或加热
的措施,观察发现样品全部溶解,溶液澄清.
(2)取少量(1)中所配溶液,加入足量的用
盐酸
盐酸
(填一种酸)酸化的氯化钡溶液有白色沉淀,说明产物中含有
SO42-
SO42-
(填离子符号).
(3)另取少量(1)中所配溶液于试管中,滴加少量盐酸,看到气泡产生,通过
招气入鼻
招气入鼻
方法闻到臭鸡蛋气味,说明生成
H2S
H2S
气体,写出生成该气体的离子反应方程式:
S2-+2H+=H2S↑
S2-+2H+=H2S↑
;同时发现溶液变浑浊,原因是:(用离子方程式表示)
SO32-+2S2-+6H+=3S↓+3H2O
SO32-+2S2-+6H+=3S↓+3H2O
.
(4)根据以上实验,该同学经分析解释了以上实验中的反常现象,请你用一个化学方程式表示:
4Na2SO3=3Na2SO4+Na2S
4Na2SO3=3Na2SO4+Na2S
.这一反应在上述实验中
否
否
(填“是”或“否”)能确定反应完全.

 +______,
+______,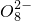 +H2O→Mn
+H2O→Mn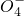 +S
+S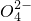 +H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
+H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol. +______,
+______,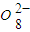 +H2O→Mn
+H2O→Mn +S
+S +H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.
+H+,该反应常用于检验Mn2+的存在.其特征现象是______,?若反应中有0.1mol还原剂参加反应,则消耗氧化剂物质的量为______mol.