
题目列表(包括答案和解析)
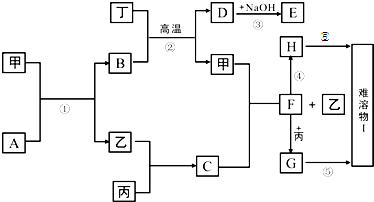
已知A、B、C、D为中学常见的气体单质,甲、乙、丙、丁为常见的化合物,甲的水溶液呈碱性。它们之间有如图所示的转化关系(部分产物及反应条件已略去)。

请回答:
 (1)乙的名称为 ,丙转化丁的离子方程式为 。
(1)乙的名称为 ,丙转化丁的离子方程式为 。
(2)实验室可通过多种方法制备甲,用右图所示装置收集甲,下列关于制取及收集甲实验的叙述正确的是 。
①甲气体不能用排水法收集
②实验室用丙一种药品可以制取甲
③右图的a为浸有稀H2SO4的棉花
|
(3)在A转化为甲的过程中,有右图所示的数据
(单位:mol/L)。在2min内A与D反应生成甲的速度V(甲)= ,2min末A的转化率为 。
(4)工业上通常以甲为原料制备HNO3。硝酸工业尾气中的NO和NO2对环境有污染,可用NaOH溶液吸收,尾气中NO与NO2按物质的量之比1:1被NaOH溶液吸收得到一种钠盐,该反应的化学方程式为 。
| ||
| ||
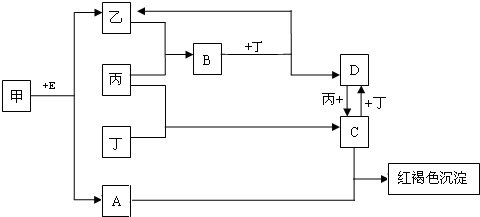
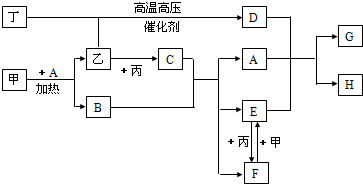
 已知A、B、D为中学常见的气体单质,甲、乙、丙、丁为常见的化合物,甲的水溶液呈碱性.它们之间有如下所示转化关系(部分产物及反应条件已略去)
已知A、B、D为中学常见的气体单质,甲、乙、丙、丁为常见的化合物,甲的水溶液呈碱性.它们之间有如下所示转化关系(部分产物及反应条件已略去)
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com