
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
£Ø19·Ö£©ĪŅ¹ś”¶³µÓĆČ¼ĮĻ¼×“¼¹ś¼Ņ±ź×¼”·µÄŹµŹ©ĄæŖĮĖ³µÓĆČ¼ĮĻµĶĢ¼øļĆüµÄ“óÄ»£¬Ņ»Š©Ź”ŹŠÕżŌŚĀ½ŠųŹŌµćÓėĶĘ¹ćŹ¹ÓĆ¼×“¼ĘūÓĶ”£¼×“¼æÉĶعż½«ĆŗµÄĘų»Æ¹ż³ĢÖŠÉś³ÉµÄCOŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦ÖĘµĆ£ŗCO(g) + 2H2(g)  CH3OH(g)”£Ķ¼I”¢Ķ¼¢ņŹĒ¹ŲÓŚøĆ·“Ó¦½ųŠŠĒéæöµÄĶ¼Ź¾”£
CH3OH(g)”£Ķ¼I”¢Ķ¼¢ņŹĒ¹ŲÓŚøĆ·“Ó¦½ųŠŠĒéæöµÄĶ¼Ź¾”£

Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ķ¼IŹĒ·“Ó¦Ź±COŗĶCH3OHµÄÅضČĖꏱ¼äµÄ±ä»ÆĒéæö£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ÓĆCOÅØ¶Č±ä»Æ±ķŹ¾Ę½¾ł·“Ó¦ĖŁĀŹv(CO)=_______________”£
£Ø2£©Ķ¼¢ņ±ķŹ¾øĆ·“Ó¦½ųŠŠ¹ż³ĢÖŠÄÜĮæµÄ±ä»Æ£¬ĒśĻßa±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŹ±·“Ó¦µÄÄÜĮæ±ä»Æ£¬ŌŚĶ¼¢ņÖŠ»³öŹ¹ÓĆ“ß»Æ¼ĮŗóµÄÄÜĮæ±ä»ÆĒśĻßb”£
£Ø3£©Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”£
£Ø4£©øĆ·“Ó¦µÄĘ½ŗā³£ŹżKµÄ±ķ“ļŹ½ĪŖ £»µ±ĪĀ¶ČÉżøߏ±£¬øĆĘ½ŗā³£ŹżK½«________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø5£©ŗćČŻĢõ¼žĻĀ£¬ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹ Ōö“óµÄÓŠ
ӣ
Ōö“óµÄÓŠ
ӣ
A£®ÉżøßĪĀ¶Č B£®³äČĖHeĘų
C£®ŌŁ³äČė1molCOŗĶ2molH2 D£®Ź¹ÓĆ“ß»Æ¼Į
£Ø6£©ŌŚŗćĪĀĢõ¼žĻĀ£¬±£³ÖCOÅØ¶Č²»±ä£¬Ą©“óČŻĘ÷Ģå»ż£¬ŌņĘ½ŗā £ØĢī”°ÄęĻņŅĘ¶Æ”±”¢”°ÕżĻņŅĘ¶Æ”±”¢”°²»ŅĘ¶Æ”±£©
£Ø7£©ŌŚĪĀ¶Č”¢ČŻ»żĻąĶ¬µÄČżøöĆܱÕČŻĘ÷ÖŠ£¬°“²»Ķ¬·½Ź½Ķ¶ĮĻ£¬±£³ÖŗćĪĀ”¢ŗćČŻ£¬²āµĆ·“Ó¦“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ
|
ČŻĘ÷ |
¼× |
ŅŅ |
±ū |
|
Ķ¶ĮĻĮæ |
1mol CO Ӣ2mol H2 |
1molCH3OH |
2molCH3OH |
|
CH3OHµÄÅØ¶Č£Ømol”¤L-1£© |
c1 |
c2 |
c3 |
|
·“Ó¦µÄÄÜĮæ±ä»Æ |
·Å³öQ1 kJ |
ĪüŹÕQ2 kJ |
ĪüŹÕQ3 kJ |
|
ĢåĻµŃ¹Ēæ£ØPa£© |
P1 |
P2 |
P3 |
|
·“Ó¦Īļ×Ŗ»ÆĀŹ |
¦Į1 |
¦Į2 |
¦Į3 |
ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ
A£®c1= c2 B£®Q3 = 2Q2 C£®2 P1£¼P3
D£®¦Į1+¦Į2=1 E£®2¦Į2=¦Į3
E£®2¦Į2=¦Į3
F£®øĆ·“Ó¦ČōÉś³É1molCH3OH·Å³öµÄČČĮæĪŖ£ØQ1+ Q2£©kJ
£Ø8£©ČōŌŚŅ»Ģå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äČė1mol CO”¢2mol H2ŗĶ1molCH3OH£¬“ļµ½Ę½ŗāŹ±²āµĆ»ģŗĻĘųĢåµÄĆܶȏĒĶ¬ĪĀĶ¬Ń¹ĻĀĘšŹ¼µÄ1.6±¶£¬ŌņøĆ·“Ó¦Ļņ £ØĢī”°Õż”±”¢”°Äę”±£©·“Ó¦·½ĻņŅĘ¶Æ£¬ĄķÓÉŹĒ
°±ŌŚ¹śĆń¾¼ĆÖŠÕ¼ÓŠÖŲŅŖµÄµŲĪ»£¬Ēė²ĪÓėĻĀĮŠĢ½¾æ”£
£Ø1£©Éś²śĒāĘų£ŗ½«Ė®ÕōĘųĶعżŗģČȵÄĢ漓²śÉśĖ®ĆŗĘų”£
C(s) + H2O(g) ![]() H2(g) + CO(g) ”÷H = +131.3 kJ £¬”÷S = +133.7 J/K
H2(g) + CO(g) ”÷H = +131.3 kJ £¬”÷S = +133.7 J/K
øĆ·“Ó¦ŌŚµĶĪĀĻĀÄÜ·ń×Ō·¢ £ØĢī£ŗÄÜ»ņ·ń£©”£
£Ø2£©ŅŃÖŖŌŚ400”ꏱ£¬N2 (g)+ 3H2(g) ![]() 2NH3(g)µÄK=0.5,
2NH3(g)µÄK=0.5,
¢Ł2NH3(g)![]() N2 (g)+ 3H2(g)µÄK= £ØĢīŹżÖµ£©”£
N2 (g)+ 3H2(g)µÄK= £ØĢīŹżÖµ£©”£
¢Ś400”ꏱ£¬ŌŚ0.5LµÄ·“ӦȯĘ÷ÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬Ņ»¶ĪŹ±¼äŗ󣬲āµĆN2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ2mol”¢1mol”¢2mol£¬Ōņ“ĖŹ±·“Ó¦V(N2)Õż V(N2)Äę£ØĢī£ŗ£¾”¢£¼”¢£½”¢²»ÄÜČ·¶Ø£©
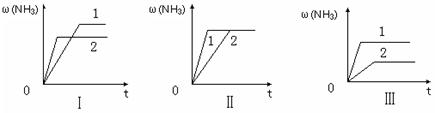
£Ø3£©ŌŚČżøöĻąĶ¬ČŻĘ÷ÖŠø÷³äČė1 molN2ŗĶ3molH2£¬ŌŚÄ³Ņ»²»Ķ¬Ģõ¼žĻĀ·“Ó¦²¢“ļµ½Ę½ŗā£¬°±µÄĢå»ż·ÖŹżĖꏱ¼ä±ä»ÆĒśĻßČēĻĀĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £ØĢīŠņŗÅ£© ”£
A£®Ķ¼¢ńæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP2£¾P1
B£®Ķ¼¢ņæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP1£¾P2
C£®Ķ¼¢óæÉÄÜŹĒ²»Ķ¬ĪĀ¶Č¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅT1£¾T2
D£®Ķ¼¢ņæÉÄÜŹĒĶ¬ĪĀĶ¬Ń¹ĻĀ£¬“߻ƼĮŠŌÄÜ£¬1£¾2
°±ŌŚ¹śĆń¾¼ĆÖŠÕ¼ÓŠÖŲŅŖµÄµŲĪ»£¬Ēė²ĪÓėĻĀĮŠĢ½¾æ”£
£Ø1£©Éś²śĒāĘų£ŗ½«Ė®ÕōĘųĶعżŗģČȵÄĢ漓²śÉśĖ®ĆŗĘų”£
C(s) + H2O(g) ![]() H2(g) + CO(g) ”÷H = +131.3 kJ/mol£¬”÷S = +133.7 J/K
H2(g) + CO(g) ”÷H = +131.3 kJ/mol£¬”÷S = +133.7 J/K
øĆ·“Ó¦ŌŚµĶĪĀĻĀÄÜ·ń×Ō·¢ ”ų £ØĢī£ŗÄÜ»ņ·ń£©”£
£Ø2£©ŅŃÖŖŌŚ400”ꏱ£¬N2 (g)+ 3H2(g) ![]() 2NH3(g) ”÷H<0 µÄK=0.5,
2NH3(g) ”÷H<0 µÄK=0.5,
¢Ł2NH3(g)![]() N2 (g)+ 3H2(g)µÄK= ”ų £ØĢīŹżÖµ£©”£
N2 (g)+ 3H2(g)µÄK= ”ų £ØĢīŹżÖµ£©”£
¢Ś400”ꏱ£¬ŌŚ0.5LµÄ·“ӦȯĘ÷ÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬Ņ»¶ĪŹ±¼äŗ󣬲āµĆN2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ2mol”¢1mol”¢2mol£¬Ōņ“ĖŹ±·“Ó¦V(N2)Õż ”ų V(N2)Äę£ØĢī£ŗ£¾”¢£¼”¢£½”¢²»ÄÜČ·¶Ø£©
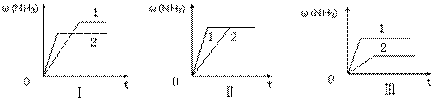
£Ø3£©ŌŚČżøöĻąĶ¬ČŻĘ÷ÖŠø÷³äČė1 molN2ŗĶ3molH2£¬ŌŚÄ³Ņ»²»Ķ¬Ģõ¼žĻĀ·“Ó¦²¢“ļµ½Ę½ŗā£¬°±µÄĢå»ż·ÖŹżĖꏱ¼ä±ä»ÆĒśĻßČēĻĀĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”ų £ØĢīŠņŗÅ£© ”£
A£®Ķ¼¢ńæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP2£¾P1
B£®Ķ¼¢ņæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP1£¾P2
C£®Ķ¼¢óæÉÄÜŹĒ²»Ķ¬ĪĀ¶Č¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅT1£¾T2
D£®Ķ¼¢ņæÉÄÜŹĒĶ¬ĪĀĶ¬Ń¹ĻĀ£¬“߻ƼĮŠŌÄÜ£¬1£¾2
£Ø8·Ö£©°±ŌŚ¹śĆń¾¼ĆÖŠÕ¼ÓŠÖŲŅŖµÄµŲĪ»£¬Ēė²ĪÓėĻĀĮŠĢ½¾æ”£
£Ø1£©Éś²śĒāĘų£ŗ½«Ė®ÕōĘųĶعżŗģČȵÄĢ漓²śÉśĖ®ĆŗĘų”£
C(s) + H2O(g) H2(g) + CO(g) ”÷H = +131.3 kJ”¤mol-1£¬”÷S =+133.7 J/K
øĆ·“Ó¦ŌŚµĶĪĀĻĀÄÜ·ń×Ō·¢ £ØĢī£ŗÄÜ»ņ·ń£©”£
£Ø2£©ŅŃÖŖŌŚ400”ꏱ£¬N2 (g)+ 3H2(g) 2NH3(g) ”÷H<0 µÄK=0.5,
¢Ł2NH3(g)N2 (g)+ 3H2(g)µÄK= £ØĢīŹżÖµ£©”£
¢Ś400”ꏱ£¬ŌŚ0.5LµÄ·“ӦȯĘ÷ÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬Ņ»¶ĪŹ±¼äŗ󣬲āµĆN2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ2mol”¢1mol”¢2mol£¬Ōņ“ĖŹ±·“Ó¦
V(N2)Õż V(N2)Äę£ØĢī£ŗ£¾”¢£¼”¢£½”¢²»ÄÜČ·¶Ø£©
£Ø3£©ŌŚČżøöĻąĶ¬ČŻĘ÷ÖŠø÷³äČė1 molN2ŗĶ3molH2£¬ŌŚÄ³Ņ»²»Ķ¬Ģõ¼žĻĀ·“Ó¦²¢“ļµ½Ę½ŗā£¬°±µÄĢå»ż·ÖŹżĖꏱ¼ä±ä»ÆĒśĻßČēĻĀĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ”” £ØĢīŠņŗÅ£© ”£
A£®Ķ¼¢ńæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP2£¾P1
B£®Ķ¼¢ņæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP1£¾P2
C£®Ķ¼¢óæÉÄÜŹĒ²»Ķ¬ĪĀ¶Č¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅT1£¾T2
D£®Ķ¼¢ņæÉÄÜŹĒĶ¬ĪĀĶ¬Ń¹ĻĀ£¬“߻ƼĮŠŌÄÜ£¬1£¾2
£Ø8·Ö£©°±ŌŚ¹śĆń¾¼ĆÖŠÕ¼ÓŠÖŲŅŖµÄµŲĪ»£¬Ēė²ĪÓėĻĀĮŠĢ½¾æ”£
£Ø1£©Éś²śĒāĘų£ŗ½«Ė®ÕōĘųĶعżŗģČȵÄĢ漓²śÉśĖ®ĆŗĘų”£
C(s) + H2O(g) 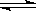 H2(g) + CO(g) ”÷H = +131.3 kJ”¤mol-1
£¬”÷S =
+133.7 J/K
H2(g) + CO(g) ”÷H = +131.3 kJ”¤mol-1
£¬”÷S =
+133.7 J/K
øĆ·“Ó¦ŌŚµĶĪĀĻĀÄÜ·ń×Ō·¢ £ØĢī£ŗÄÜ»ņ·ń£©”£
£Ø2£©ŅŃÖŖŌŚ400”ꏱ£¬N2 (g)+ 3H2(g) 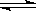 2NH3(g) ”÷H<0 µÄK=0.5,
2NH3(g) ”÷H<0 µÄK=0.5,
¢Ł2NH3(g)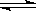 N2 (g)+ 3H2(g)µÄK= £ØĢīŹżÖµ£©”£
N2 (g)+ 3H2(g)µÄK= £ØĢīŹżÖµ£©”£
¢Ś400”ꏱ£¬ŌŚ0.5LµÄ·“ӦȯĘ÷ÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬Ņ»¶ĪŹ±¼äŗ󣬲āµĆN2”¢H2”¢NH3µÄĪļÖŹµÄĮæ·Ö±šĪŖ2mol”¢1mol”¢2mol£¬Ōņ“ĖŹ±·“Ó¦
V(N2)Õż V(N2)Äę£ØĢī£ŗ£¾”¢£¼”¢£½”¢²»ÄÜČ·¶Ø£©
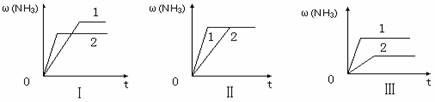
£Ø3£©ŌŚČżøöĻąĶ¬ČŻĘ÷ÖŠø÷³äČė1 molN2ŗĶ3molH2£¬ŌŚÄ³Ņ»²»Ķ¬Ģõ¼žĻĀ·“Ó¦²¢“ļµ½Ę½ŗā£¬°±µÄĢå»ż·ÖŹżĖꏱ¼ä±ä»ÆĒśĻßČēĻĀĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”” £ØĢīŠņŗÅ£© ”£
A£®Ķ¼¢ńæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP2£¾P1
B£®Ķ¼¢ņæÉÄÜŹĒ²»Ķ¬Ń¹Ēæ¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅP1£¾P2
C£®Ķ¼¢óæÉÄÜŹĒ²»Ķ¬ĪĀ¶Č¶Ō·“Ó¦µÄÓ°Ļģ£¬ĒŅT1£¾T2
D£®Ķ¼¢ņæÉÄÜŹĒĶ¬ĪĀĶ¬Ń¹ĻĀ£¬“߻ƼĮŠŌÄÜ£¬1£¾2
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com