
题目列表(包括答案和解析)
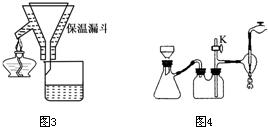 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.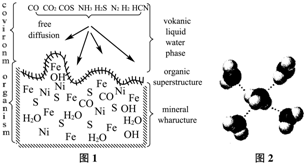
| 电离能/kJ?mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |


(10分)目前世界上60%的镁是从海水中提取的,下图是某工厂从海水中提取镁的主要步骤。学生就这个课题展开了讨论。学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集
有三个学生提出自己的观点。
学生甲的观点:直接往海水中加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
通过分析比较你认为学生 的观点正确(填学生序号),简述理由: 。
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,并充分利用当地的贝壳(主要成分为碳酸钙)资源,加入的足量试剂①是 (填化学式)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 (填标号字母)
A.蒸馏 B.过滤 C.萃取 D.分液
(3)加入的足量试剂②是 (填化学式)。
(4)写出由无水MgCl2制取金属镁的化学方程式
下面是几种实验中常用的仪器:
A. B.
B. C.
C. D.
D.
(1)写出序号所代表的仪器的名称:B___________;C___________;D___________
实验室要配制500 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(2)用托盘天平称取氢氧化钠,其质量为_______________g。
(3)下列主要操作步骤的正确顺序是_______________(填序号)。
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②“定容”
③待冷却至室温后,将溶液转移到500 mL 容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2—3次,洗涤液转移到容量瓶中。
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配浓度偏高的是__________。
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
(5)写出步骤②“定容”的具体操作:
(6)海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。某学生课
外活动小组欲从海藻中提取碘,设计如下的流程:
(已知过程②中反应的离子方程式为:2I- + Cl2 = 2Cl- + I2)

Ⅰ.指出提取碘的过程中有关的实验操作的名称:① , ③ 。
Ⅱ.提取碘的过程中,可选择的有机溶剂是 (填序号) 。
A、酒精 B、醋酸 C 、四氯化碳
糖尿病的致病原因之一是缺乏胰岛素,主要表现为血糖增高。合理的饮食是治疗糖尿病的基础,肥胖者要限制热量,减轻体重;消瘦者要有足够的热量以恢复理想的体重。饮食中碳水化合物所提供的热量不要高于总热量的55%—60%,胆固醇每日摄入量要低于300 mg,糖的食用要有节制。(资料来源:《中国大百科全书》)
食 谱
早餐:馒头、绿豆粥、黄瓜拌虾皮 午餐:清椒牛肉丝、炒菠菜、紫菜蛋汤、米饭 晚餐:清煮河鳗、焖扁豆、米饭 |
专家对该类病人每日主要营养成分的推荐摄入量和食谱的实测数据见下表
名称 | 专家推荐摄入量 | 图中食谱实测数据 |
蛋白质/g | 93 | 80 |
脂肪/g | 70 | 50 |
碳水化合物/g | 330 | 450 |
总热量/kJ | 9 851 | 10 910 |
(1)已知每克蛋白质、脂肪、碳水化合物分别产生17 kJ、38 kJ、17 kJ热量,该食谱中蛋白质、脂肪和碳水化合物所提供的热量占总热量的百分比分别是_____________、_____________和_____________。
(2)通过对上题数据的分析,小王得到的结论是____________________________________。
(3)如果要对该食谱进行较为全面的分析,还需要的数据有_____________、_____________。
(4)小王对食谱的评价过程包括_____________、_____________和得出结论三个环节。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com