
题目列表(包括答案和解析)
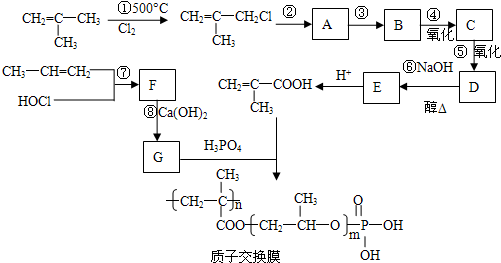
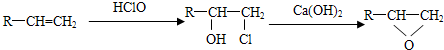
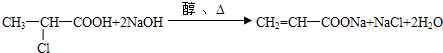

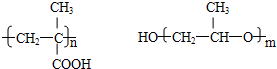 它们的物质的量之比为
它们的物质的量之比为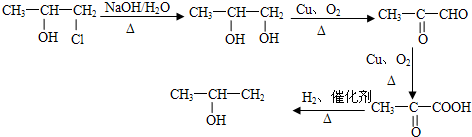

 (2009?丹东模拟)请根据工业制硫酸的有关知识回答下列问题:
(2009?丹东模拟)请根据工业制硫酸的有关知识回答下列问题:
| ||
| ||
| ||
| △ |


煤的直接燃烧已引起严重的生态和环境污染,并且其直接燃烧很难解决温室气体减排问题。解决煤炭的清洁高效利用问题是中国发展低碳经济的关键。下图是煤气化和除硫的实验系统示意图:
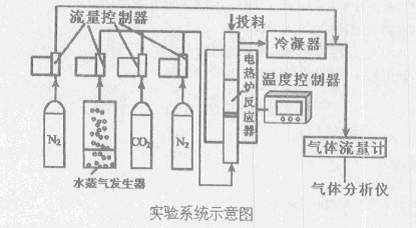
其操作步骤为:
I.升温至实验温度,通人高纯N2,从投料口加人石英砂(含载氧体)
Ⅱ.停止通入N2,从反应器下方按比例通入水蒸气和CO2,从投料口加入CaO
Ⅲ.停止通入水蒸气和CO2,从投料口加入煤
Ⅳ.持续通入水蒸气和CO2,开始反应;在气体出口管中通人高纯N2
(1)冷凝器的作用是 。
(2)可使用CaCO3代替CaO脱硫,CaCO3脱硫的化学方程式为 。
(3)通人N2的目的: 。
(4)反应器中发生如下几种反应:
C(s)十H2O(g)=CO(g)+H2(g) △H=+131kJ/mol
C(s)+O2(g)=CO2(g) △H=-394kJ/mol
CO(g)+ O2(g)=CO2(g) △H=-283kJ/mol
O2(g)=CO2(g) △H=-283kJ/mol
CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
下图能表示CO与H2O(g)生成CO2和H2的反应过程和能量关系的图是 (填序号)。
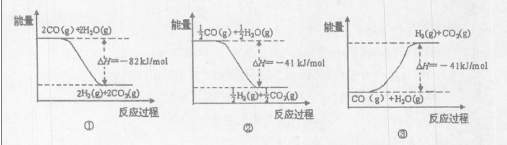
(5)已知830℃时,CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数K=1,等物质的量的CO和H2O反应达到平衡时,CO的转化率为
.
H2(g)+CO2(g)的平衡常数K=1,等物质的量的CO和H2O反应达到平衡时,CO的转化率为
.
(6)煤气化过程中会生成少量CH4,已知CH4与CaSO4反应生成CaS、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为 。
(7)煤气化后,混合气体由CO、H2和CH4等组成,可用于制燃料电池。其中碱性条件下CH4参与反应的电极反应式为 。
(14分)I.在化学实验时必须注意安全操作,避免意外伤害,下列实验操作或事故处理不正确的是 ( )
①在点燃易燃气体前,必须检验气体的纯度
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌
③浓硫酸对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸稀溶液
④给试管中的液体加热时,液体不超过试管容积的1/3
⑤点燃添满酒精的酒精灯
⑥实验时不慎被玻璃划破手指,引起轻微流血时,用三氯化铁溶液涂抹止血(血液可看作是胶体分散系)
II.某同学用胆矾晶体(CuSO4·5H2O )配制0.40mol/L的CuSO4溶液240mL,回答下列问题
(1)所需仪器为:托盘天平、药匙、烧杯、 胶头滴管 ,还需要哪些玻璃仪器才能完成该实验,请写出: 。
(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾 g ③ ④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀
(3)下图是该同学转移溶液的示意图,图中的错误是 。

(4)该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响 (填“偏高”、“偏低”或“无影响”)。
(5)一瓶配制好的稀CuSO4溶液,因时间过长,标签污损,为检验它就是盛有CuSO4溶液,说说你的实验检验方法。
|
鉴别对象 |
实验操作、现象 |
|
Cu2+ |
|
|
|
|
(15分)硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工产品发展重点”之一。下图是某种品位的石英砂矿石(主要成分是SiO2,还含有一定量的Fe2O3、Na2SO4、Na2CO3等杂质)制备硅酸钠的工艺流程示意简图:

阅读上述资料,回答下列问题
(1)作为“我国优先发展的精细化学品”,硅酸钠用途很多,请列举一个硅酸钠的用途
(2)石英矿粉用水淋洗,检验洗出液中含有SO42—的实验操作和实验现象分别是:用胶头滴管取2ml洗出液I于试管中,
(3)在操作I得到的滤渣中加入烧碱溶液,请写出反应的离子方程式
(4)“操作I”的名称为
“操作II”包含“蒸发浓缩、冷却结晶、过滤”系列操作,其中“蒸发浓缩”所用到的硅酸盐
材料的仪器有
(5)“取样分析”的目的是确保滤渣II中不含有杂质离子,简述“取样分析”的操作和实验现象:用胶头滴管取2ml洗出液II于试管中,
(6)下列关于Si、SiO2、Na2SiO3等物质的说法,不正确的是
| A.硅在周期表的位置是第三周期第IVA族 |
| B.原子半径大小关系:Na > Si > C > O |
| C.二氧化硅是酸性氧化物,能与强碱反应,不与任何酸反应 |
| D.实验室烧熔烧碱固体采用的仪器有酒精灯、玻璃棒、石英坩埚 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com