A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如

下图所示(反应条件均已略去).
请回答下列问题:
(1)D的化学式为
H2
H2
;
(2)反应③的离子方程式为
3NO2+H2O═2H++2NO3-+NO
3NO2+H2O═2H++2NO3-+NO
.
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
.
(4)0.1mol/L的X溶液和0.1mol/L的Y溶液等体积混合,溶液呈
酸性
酸性
性;(填“酸”、“碱”或“中”)该溶液中各离子浓度大小关系为:
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
.
(5)常温下0.1mol/L的Y溶液中c(H
+)/c(OH
-)=1×10
-8,下列叙述正确的是
ACD
ACD
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度0.1mol/L
C.该溶液中水电离出的c(H
+)与c(OH
-)乘积为1×10
-22D. pH=3的盐酸溶液V
1 L与该0.1mol/L的Y溶液V
2 L混合,若混合溶液pH=7,则:V
1>V
2E.将pH=11的Y溶液加水稀释100倍后,pH值为9;
(6)化合物E在一定条件下于一定体积的容器中可发生身氧化还原反应,测得容器内气体的压强略小于原来的2/3,请写出该反应的化学方程式
3NO═NO2+N2O
3NO═NO2+N2O
.

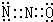
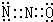
 下图所示(反应条件均已略去).
下图所示(反应条件均已略去). 如图是一些重要工业生产的转化关系(反应条件略去):
如图是一些重要工业生产的转化关系(反应条件略去):

 N2O↑+2H2O
N2O↑+2H2O K2MnO4+MnO2+O2 ↑ ④S+2KNO3+3C
K2MnO4+MnO2+O2 ↑ ④S+2KNO3+3C K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑ Hg+SO2
Hg+SO2