
题目列表(包括答案和解析)

复分解反应探究的是酸、碱、盐等化合物在溶液中相互反应的情况。回答下列问题:
书写方程式:
①氢氧化钠溶液与稀盐酸混合:____________________________________________;
②碳酸钠溶液与足量稀盐酸混合:__________________________________________;
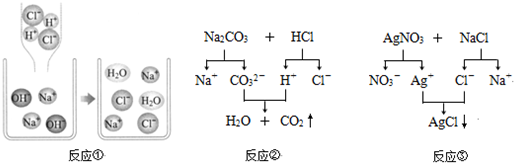
上述反应的微观图解如右图所示:
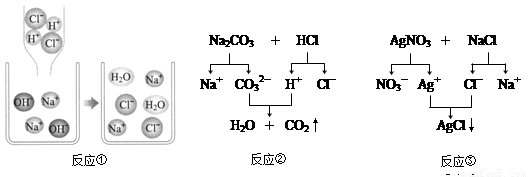
反应①的实质是H+和OH-结合生成水,Cl-和Na+没有发生变化;反应②的实质是H+和CO32-结合生成水和二氧化碳,Cl-和Na+没有发生变化,则反应③的实质是_________和__________生成AgCl。所以复分解反应的实质是某些阴、阳离子结合生成水或气体或____________的过程;
构建短线相连的下列离子对,在方框内填写相应的离子符号,要求构成的离子对能符合复分解反应的实质。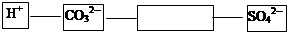
| A.碱溶液都显碱性,则碱性溶液一定是碱溶液 |
| B.离子是带电的原子或原子团,所以带电的微粒一定是离子 |
| C.化合物都是由不同种元素组成的,但不同种元素组成的物质不一定是化合物 |
| D.催化剂在化学反应中质量和化学性质都不改变,则在化学反应中质量和化学性质都不改变的物质一定是该反应的催化剂 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com