(1)甲烷的部分氧化反应如下:2CH
4(g) +O
2(g)=2CO(g) +4H
2(g) △H=-71.2 kJ/mol
有研究认为甲烷部分氧化的机理为:
①CH
4(g)+2O
2(g)=CO
2(g)+2H
2O(g) △H1=- 890.3 kJ/mol
②CH
4(g)+CO
2(g)=2CO(g)+2H
2(g) △H2
③CH
4(g)+H
2O(g)=CO(g) +3H
2(g) △H3=+250.3 kJ/mol 则△H2=____。
(2)催化反应室1中合成甲醚的反应为:2CO(g)+4H
2(g)

CH
3OCH
3(g)+H
2O(g),该反应为自发反应,则该反应的△H___________(填“<”、“>”或“=”)0。
(3)催化反应室2中发生如下反应:CO(g) +2H
2(g)
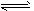
CH
3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H
2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图a所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___;都达到化学平衡状态时,CO转化率最低的是___。
(4)如图b为熔融碳酸盐燃料电池的工作原理示意图。熔融碳酸盐燃料电池的正极反应式可表示为:____。





 CH3OCH3(g)+H2O(g),该反应为自发反应,则该反应的△H___________(填“<”、“>”或“=”)0。
CH3OCH3(g)+H2O(g),该反应为自发反应,则该反应的△H___________(填“<”、“>”或“=”)0。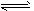 CH3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图a所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___;都达到化学平衡状态时,CO转化率最低的是___。
CH3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时CO的体积分数如图a所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是___;都达到化学平衡状态时,CO转化率最低的是___。 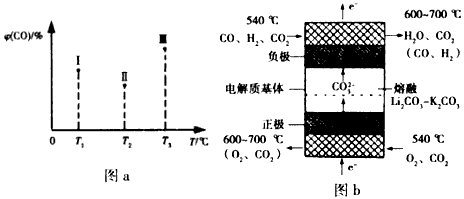
 通过煤的气化和液化,使碳及其化合物得以广泛应用.
通过煤的气化和液化,使碳及其化合物得以广泛应用.