
题目列表(包括答案和解析)
(每空2分,共10分)(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是_____
A、KMnO4 B、 H2O2 C、 Cl2水 D、 HNO3
然后再继续加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+
而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C.CuO D. Cu(OH)2
(2)向25 mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,得到曲线如下图所示
①、写出氢氧化钠溶液与醋酸溶液反应的离子方程式
②、该氢氧化钠溶液的物质的量浓度为
③、在B点,a 12.5 mL(填“大于”、“小于”或“等于”)
(每空2分,共10分)(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是_____
A、KMnO4 B、 H2O2 C、 Cl2水 D、 HNO3
然后再继续加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+
而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)向25 mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,得到曲线如下图所示 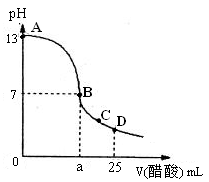
①、写出氢氧化钠溶液与醋酸溶液反应的离子方程式
②、该氢氧化钠溶液的物质的量浓度为
③、在B点,a 12.5 mL(填“大于”、“小于”或“等于”)
(每空2分,共10分)(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是_____
A、KMnO4 B、 H2O2 C、 Cl2 水 D、 HNO3
然后再继续加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+
而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)向25 mL氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,得到曲线如下图所示
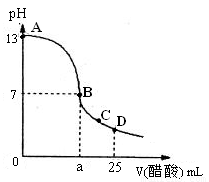
①、写出氢氧化钠溶液与醋酸溶液反应的离子方程式
②、该氢氧化钠溶液的物质的量浓度为
③、在B点,a 12.5 mL(填“大于”、“小于”或“等于”)
(每空2分,共30分)利用“化学计量在实验中的应用”的相关知识进行填空
(1)0.2 mol NH3气体中含的NH3分子数是 ,其中含氢原子数是 ,含有电子的物质的量是 .
(2)1摩尔Ba(OH)2固体中含有的Ba2+的个数是 ,全部溶于水,电离产生的OH-的物质的量是 mol,通入二氧化碳气体,恰好完全反应,消耗的二氧化碳的物质的量是 摩尔。
(3)H2SO4的摩尔质量是 ,49gH2SO4中含有 mol氧原子,含有氢的质量是 。
能与 摩尔NaOH恰好完全反应,生成水的质量是 克。
(4)含有6.02×1023个氧原子的H3pO4的物质的量是_________?
(5)与标准状况下VLCO2所含氧原子数目相同的水的质量是________(用分式表示)
(6)将4 g NaOH溶解在10 mL水中,再稀释成1 L,从中取出10 mL,这10 mL溶液
的物质的量浓度为__________________
(7)在一定的温度和压强下,1体积X2 (g)跟3体积Y2 (g)化合生成2体积化合物,则该化合物的化学式是_______________
(每空2分,共10分)
四川汶川盛产品质优良的甜樱桃。甜樱桃中含有一种羟基酸(用A表示)。A的碳链结构无支链,化学式为C4H6O5;1.34g A与足量的NaHCO3溶液反应,生成标准状况下的气体0.448 L。A在一定条件下可发生如下转化:

 其中:B、C、D、E分别代表一种直链有机物,它们的碳原子数相等。E的化学式为C4H6O6 (转化过程中生成的其它产物略去)。
其中:B、C、D、E分别代表一种直链有机物,它们的碳原子数相等。E的化学式为C4H6O6 (转化过程中生成的其它产物略去)。
已知:


 A的合成方法如下:
A的合成方法如下:

 其中,F、G、M分别代表一种有机物。
其中,F、G、M分别代表一种有机物。
请回答下列问题:
 (1)A的结构简式是_____________________。
(1)A的结构简式是_____________________。
(2)C生成D的化学方程式是 。
 (3)A与乙醇混合发生分子间脱水,可能生成的有机物共有 种。
(3)A与乙醇混合发生分子间脱水,可能生成的有机物共有 种。
(4)F的结构简式是 。
 (5)写出G与H2O反应生成A和M的化学方程式: 。
(5)写出G与H2O反应生成A和M的化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com