
题目列表(包括答案和解析)
A.H2S、SO2 B.O
标准状况下H2S和O2的混合气体100 mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10 mL,该10 mL气体可能是( )
A.H2S、SO2 B.O2 C.H2S D.SO3
标准状况下H2S和O2的混合气体100 mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10 mL,该10 mL气体可能是
A.H2S、SO2 B.O2 C.H2S D.SO3
 2SO3(g) △H<0。下列说法中正确的是_________。
2SO3(g) △H<0。下列说法中正确的是_________。 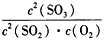 保持不变时,反应达到平衡状态
保持不变时,反应达到平衡状态 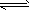 2SO3(g) △H= -Q kJ/mol(Q>0) 。
2SO3(g) △H= -Q kJ/mol(Q>0) 。 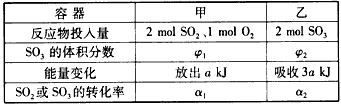
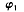 _____
_____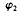 (填“>”“<”“=”),
(填“>”“<”“=”),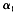 +
+ =_______
=_______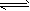 2SO3(g)达平衡后,再向乙中加入0.5 mol SO2、0.25 mol O2、1.5 mol SO3,平衡
2SO3(g)达平衡后,再向乙中加入0.5 mol SO2、0.25 mol O2、1.5 mol SO3,平衡硫有多种化合物,许多含硫化合物在工业上有重要的用途。
(1)工业上可用黄铁矿、焦炭在有限的空气中燃烧制备硫磺。
3FeS2 + 12C+ 8O2  Fe3O4 + nA↑+ 6S
Fe3O4 + nA↑+ 6S
A是 (写化学式)。若得到192克的硫磺,则产生标准状况下的A气体 L。
(2)硫的氯化物常做橡胶工业的硫化剂。硫与氯气在一定条件下反应,得到两种硫的氯化物B和D。B物质中的含硫量为0.3107,D物质中的含氯量为0.5259,B的相对分子质量比D小32。计算确定这两种氯化物的分子式分别为 。
(3)硫化氢有毒。在120℃、101kPa,将H2S和O2在密闭容器中点燃,充分反应后又恢复到了原来的温度和压强时,气体体积减少30%,求原混合其气体中H2S的体积分数。写出推导过程。(不考虑硫化氢的分解)
(4)硫代硫酸钠是重要的还原剂,可用亚硫酸钠和硫粉在水溶液中加热制得。取15.12g Na2SO3溶于80.0mL水中,加入5.00g硫粉,用小火加热至微沸,反应约1小时后过滤,将滤液蒸发至体积为30.0mL,再冷却到10℃,则理论上析出Na2S2O3?5H2O多少克?写出推导过程。(已知:Na2S2O3的溶解度,10℃时为60.0g/100g水,100℃时为207g/100g水。100℃时,Na2S2O3饱和溶液的密度为1.14g/mL)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com