
题目列表(包括答案和解析)
金属越活泼,则( )
A.其单质的还原性越强
B.其原子在化学反应中失去电子越多
C.其阳离子的氧化性越弱
D.其阳离子的还原性越强
A.其单质的还原性越强
B.其原子在化学反应中失去电子越多
C.其阳离子的氧化性越弱
D.其阳离子的还原性越强
| 实验步骤 | 实验现象 | 实验结论及离子方程式 |
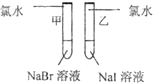 |
甲 溶液由无色变为橙色 溶液由无色变为橙色 乙 溶液由无色变为黄色 溶液由无色变为黄色 |
离子方程式 甲: 2Br-+Cl2═Br2+2Cl- 2Br-+Cl2═Br2+2Cl- 乙: 2I-+Cl2═2Cl-+I2 2I-+Cl2═2Cl-+I2 结论:卤素单质的氧化强到弱的顺序为Cl2>Br2>I2 |
| 实验步骤 | 实验现象 | 实验依据和结论 |
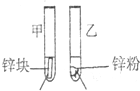 3mL1mol/L 3mL3mol/L 盐酸 盐酸 (金属质量相同,盐酸均过量) |
均有气体生成,锌粉先消失,锌块后消失 | 因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快. |

下面叙述正确的是( )
A.同族非金属元素,自上而下所形成的酸,其酸性渐弱,因为成酸元素的非金属性渐弱
B.同族非金属的最低价阴离子,由上而下其还原性渐强,而氧化性渐弱
C.同主族元素的单质,金属则越向下熔点基本上越低,非金属则越高
D.元素周期表中Ⅲ B族的元素种类最多
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com