
题目列表(包括答案和解析)
|
甲酸的下列性质中,不能证明它是弱电解质的是 | |
| [ ] | |
A. |
1 mol·L-1 甲酸溶液的pH值约为2 |
B. |
甲酸电离出的阳离子全部是H+ |
C. |
10 mL 1 mol·L-1 甲酸与10 mL 1 mol·L-1 NaOH溶液完全反应后,溶液呈碱性 |
D. |
含 [H+]1 mol·L-1甲酸溶液100 mL和足量Zn反应放出标准状况下H2的体积大于1.12 L |
( 8分)已知氨水的电离度与醋酸的电离度在同温同浓度下相等,溶有一定量氨的氯化铵溶液呈碱性。现向少量的Mg(OH)2悬浊液中,加入适量的饱和氯化铵溶液,固体完全溶解。
甲同学的解释是:Mg(OH)2(固)Mg2+(aq)+2OH—(aq)…………①
NH4++H2ONH3·H2O +H+…………② H++OH―
H2O…………③
由于NH4+水解显酸性,H+与OH―反应生成水,导致反应①平衡右移,沉淀溶解;
乙同学的解释是:Mg(OH)2(固)Mg2+(aq)+2OH—(aq)……① NH4++OH―
NH3·H2O……②
由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH―结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是 (填写编号)。
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3·H2O
(2)请你说明丙同学作出该选择的理由 。
(3)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理 (填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式 。
(12分)甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下: 甲:①准确配制0.1mol·L-1的HA、HCl溶液各100 mL;
②取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1 mol·L-1的 HA 、HCl溶液各10 mL,按图装好,观察现象
乙:①用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
②再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/20 mL)分别稀释至100mL,再用pH计测其pH变化
(1) 甲、乙两方案中都要用到__________ mL的容量瓶。乙方案中说明HA是弱电解质的理由是,测得0.1 mol·L-1的HA溶液的pH 1(填“>”、“<”或“=”) ;甲方案中,说明HA是弱电解质的实验现象是:
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第______步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1 mol/L的HA溶液中,选择加入_________试剂;②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol/L的HA溶液中,选择加入________试剂。
A. NaA固体(可完全溶于水) B.1 mol/LNaOH溶液
C. 1 mol/L H2SO4 D.2 mol/LHA
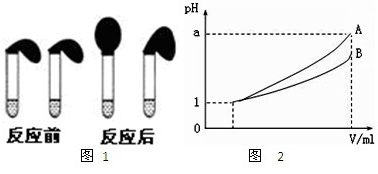
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示。
则下列说法不正确的有( )。
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com