
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
“—÷™∂Ã÷İ∆Ğ÷˜◊‘™ÀÿX°¢Y°¢Z°¢W£¨‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û«“X∫ÕYµƒ‘≠◊”–Ú ˝÷Æ∫Õµ»”ĞZµƒ‘≠◊”–Ú ˝£¨X∫ÕZø…–Œ≥…X2Z£¨X2Z2¡Ω÷÷ªØ∫œŒÔ£¨W «∂Ã÷İ∆Ğ÷˜◊‘™Àÿ÷–∞Îæ∂◊Ó¥Ûµƒ‘™Àÿ£Æ
(1)W‘Ğ÷İ∆бÌ÷–µƒŒª÷√£∫________£Æ
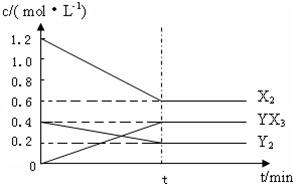
(2)‘Ğ“ª∂®Ãº˛œ¬£¨»ıª˝Œ™1 L√ݱ’»ı∆˜÷–º”»Î1.2 mol°°X2∫Õ0.4 mol°°Y2£¨∑¢…˙»Áœ¬∑¥”¶£∫3X2(g)£´Y2(g)![]() 2YX3(g)°°¶§H∑¥”¶∏˜ŒÔ÷ µƒ¡ø≈®∂»ÀÊ ±º‰±‰ªØ»Áœ¬£∫
2YX3(g)°°¶§H∑¥”¶∏˜ŒÔ÷ µƒ¡ø≈®∂»ÀÊ ±º‰±‰ªØ»Áœ¬£∫
¢Ÿ¥À∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™________(”√ªØ—ß Ω±Ì æ)£¨K£Ω________£Æ
¢Ğ»Ù…˝∏şŒ¬∂»∆Ω∫‚≥£ ˝Kº–°£¨‘Ú¶§H________0(Ãӣ棨£º)£Æ
(3)A1 «Àƒ÷÷‘™Àÿ÷–»˝÷÷‘™Àÿ◊È≥…µƒµÁΩ‚÷ £¨»İ“∫≥ ºÓ–‘£¨Ω´0.1 mol°§L£≠1µƒA1»İ“∫œ° Õ÷¡‘≠ê˝µƒ10±∂∫ۻݓ∫µƒpH£Ω12£¨‘ÚA1µƒµÁ◊” ΩŒ™________£Æ
(4)B1°¢B2 «”…Àƒ÷÷‘™Àÿ»˝÷÷–Œ≥…µƒ«øµÁΩ‚÷ £¨«“»İ“∫≥ À·–‘£¨œ‡Õ¨≈®∂» ±B1»İ“∫÷–ÀƵƒµÁ¿Î≥Ã∂»–°”ĞB2»İ“∫÷–ÀƵƒµÁ¿Î≥Ã∂»£¨∆‰‘≠“Ú «________£Æ
(5)A2∫ÕB1∑¥”¶…˙≥…B2£¨‘Ú0.2 mol/L°°A2∫Õ0.1 mol/L°°B1µ»Ãª˝ªÏ∫œ∫ۻݓ∫÷–¿Î◊”≈®∂»¥Û–°πÿœµŒ™________£Æ
“—÷™∂Ã÷İ∆Ğ÷˜◊‘™ÀÿX°¢Y°¢Z°¢W£¨‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û«“X∫ÕYµƒ‘≠◊”–Ú ˝÷Æ∫Õµ»”ĞZµƒ‘≠◊”–Ú ˝£¨X∫ÕZø…–Œ≥…X2Z£¨X2Z2¡Ω÷÷ªØ∫œŒÔ£¨W «∂Ã÷İ∆Ğ÷˜◊‘™Àÿ÷–∞Îæ∂◊Ó¥Ûµƒ‘™Àÿ£Æ
(1)W‘Ğ÷İ∆бÌ÷–µƒŒª÷√£∫________£Æ
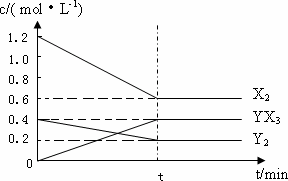
(2)‘Ğ“ª∂®Ãº˛œ¬£¨»ıª˝Œ™1 L√ݱ’»ı∆˜÷–º”»Î1.2 mol°°X2∫Õ0.4 mol°°Y2£¨∑¢…˙»Áœ¬∑¥”¶£∫3X2(g)£´Y2(g)![]() 2YX3(g)°°¶§H∑¥”¶∏˜ŒÔ÷ µƒ¡ø≈®∂»ÀÊ ±º‰±‰ªØ»Áœ¬£∫
2YX3(g)°°¶§H∑¥”¶∏˜ŒÔ÷ µƒ¡ø≈®∂»ÀÊ ±º‰±‰ªØ»Áœ¬£∫
¢Ÿ¥À∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™________(”√ªØ—ß Ω±Ì æ)£¨K£Ω________£Æ
¢Ğ»Ù…˝∏şŒ¬∂»∆Ω∫‚≥£ ˝Kº–°£¨‘Ú¶§H________0(Ãӣ棨£º)£Æ
(3)A1 «Àƒ÷÷‘™Àÿ÷–»˝÷÷‘™Àÿ◊È≥…µƒµÁΩ‚÷ £¨»İ“∫≥ ºÓ–‘£¨Ω´0.1 mol°§L£≠1µƒA1»İ“∫œ° Õ÷¡‘≠ê˝µƒ10±∂∫ۻݓ∫µƒpH£Ω12£¨‘ÚA1µƒµÁ◊” ΩŒ™________£Æ
(4)B1°¢B2 «”…Àƒ÷÷‘™Àÿ»˝÷÷–Œ≥…µƒ«øµÁΩ‚÷ £¨«“»İ“∫≥ À·–‘£¨œ‡Õ¨≈®∂» ±B1»İ“∫÷–ÀƵƒµÁ¿Î≥Ã∂»–°”ĞB2»İ“∫÷–ÀƵƒµÁ¿Î≥Ã∂»£¨∆‰‘≠“Ú «________£Æ
(5)A2∫ÕB1∑¥”¶…˙≥…B2£¨‘Ú0.2 mol/L°°A2∫Õ0.1 mol/L°°B1µ»Ãª˝ªÏ∫œ∫ۻݓ∫÷–¿Î◊”≈®∂»¥Û–°πÿœµŒ™________£Æ
A°¢B°¢D°¢EÀƒ÷÷‘™Àÿæ˘Œ™∂Ã÷İ∆Ğ‘™Àÿ£¨‘≠◊”–Ú ˝÷Ω•‘ˆ¥Û°£A‘™Àÿ‘≠◊”µƒ∫ÀÕ‚µÁ◊” ˝°¢µÁ◊”≤„ ˝∫Õ◊ÓÕ‚≤„µÁ◊” ˝æ˘œ‡µ»°£B°¢D°¢E»˝÷÷‘™Àÿ‘Ğ÷İ∆бÌ÷–œ‡∂‘Œª÷√»ÁÕº¢Ÿ£¨÷ª”–E‘™Àÿµƒµ•÷ ƒİ”ÎÀÆ∑¥”¶…˙≥…¡Ω÷÷À·°£º◊°¢““°¢M°¢W°¢X°¢Y°¢Z∆ş÷÷ŒÔ÷ æ˘”…A°¢B°¢D»˝÷÷‘™Àÿ÷–µƒ“ª÷÷ªÚº∏÷÷◊È≥…£¨∆‰÷–÷ª”–M∑÷◊”Õ¨ ±∫¨”–»˝÷÷‘™Àÿ£ªWŒ™A°¢B¡Ω‘™Àÿ◊È≥…µƒ18µÁ◊”∑÷◊”£¨ø…◊ˆªº˝»º¡œ£ªº◊°¢““Œ™∑«Ω Ùµ•÷ £ªX∑÷◊”∫¨”–10∏ˆµÁ◊”°£À¸√«÷ƺ‰µƒ◊™ªØπÿœµ»ÁÕº¢Ğ°£
 |
ªÿ¥œ¬¡–Œ £∫
°° (1)ZµƒªØ—ß ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°° £ª
°° (2)Eµƒµ•÷ ”ÎÀÆ∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°° £ª
(3)W8ø’∆¯»º¡œµÁ≥ÿ «“ª÷÷ºÓ–‘»º¡œµÁ≥ÿ£¨µÁΩ‚÷ »İ“∫ «20©á°´30©áµƒKOH»İ“∫°£W8ø’∆¯»º¡œµÁ≥ÿ∑≈µÁ ±£¨’˝º´∑¥”¶ ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°° £¨∏∫º´∑¥”¶ ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£ª
°° (4)Ω´“ª∂®¡øµƒA2°¢B2µƒªÏ∫œ∆¯ÃÂ∑≈»Î1L±’√İ»ı∆˜÷–£¨‘Ğ500°Ê°¢2°¡107paœ¬¥ÔµΩ∆Ω∫‚°£≤‚µ√∆Ω∫‚∆¯Ãµƒ◊İŒÔ÷ µƒ¡øŒ™0.50mol£¨∆‰÷–A2Œ™0.3mol£¨B2Œ™0.1mol°£‘Ú∏√ú˛œ¬A2µƒ∆Ω∫‚◊™ªØ¬ Œ™°°°°°°°°°°°°°°°° £¨∏√Œ¬∂»œ¬µƒ∆Ω∫‚≥£ ˝Œ™°°°°°°°°°°°°°°°° °£
(11∑÷)“—÷™∂Ã÷İ∆Ğ÷˜◊‘™ÀÿX°¢Y°¢Z°¢W£¨‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û«“X∫ÕYµƒ‘≠◊”–Ú ˝÷Æ∫Õµ»”ĞZµƒ‘≠◊”–Ú ˝£¨X∫ÕZø…–Œ≥…X2Z£¨X2Z2¡Ω÷÷ªØ∫œŒÔ£¨W «∂Ã÷İ∆Ğ÷˜◊‘™Àÿ÷–∞Îæ∂◊Ó¥Ûµƒ‘™Àÿ°£
¢≈W‘Ğ÷İ∆бÌ÷–µƒŒª÷√£∫ °£
¢∆‘Ğ“ª∂®Ãº˛œ¬£¨»ıª˝Œ™1L√ݱ’»ı∆˜÷–º”»Î1.2molX2∫Õ0.4molY2£¨∑¢…˙»Áœ¬∑¥”¶£∫
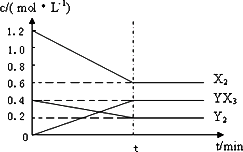
3X2 (g) + Y2(g) 2YX3(g) °˜H ∑¥”¶∏˜ŒÔ÷ µƒ¡ø≈®∂»ÀÊ ±º‰±‰ªØ»Áœ¬£∫
¢Ÿ¥À∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™ (”√ªØ—ß Ω±Ì æ) £¨ K= °£
¢Ğ»Ù…˝∏şŒ¬∂»∆Ω∫‚≥£ ˝Kº–°£¨‘Ú°˜H 0(Ãӣ棨£º)°£
¢«A1 «Àƒ÷÷‘™Àÿ÷–»˝÷÷‘™Àÿ◊È≥…µƒµÁΩ‚÷ £¨»İ“∫≥ ºÓ–‘£¨Ω´0.1mol°§L-1µƒA1»İ“∫œ° Õ÷¡‘≠ê˝µƒ10±∂∫ۻݓ∫µƒpH=12£¨‘ÚA1µƒµÁ◊” ΩŒ™ °£
¢»B1°¢B2 «”…Àƒ÷÷‘™Àÿ»˝÷÷–Œ≥…µƒ«øµÁΩ‚÷ £¨«“»İ“∫≥ À·–‘£¨œ‡Õ¨≈®∂» ±B1»İ“∫÷–ÀƵƒµÁ¿Î≥Ã∂»–°”ĞB2»İ“∫÷–ÀƵƒµÁ¿Î≥Ã∂»£¨∆‰‘≠“Ú « °£
¢…A2∫ÕB1∑¥”¶…˙≥…B2£¨‘Ú0.2mol/LA2∫Õ0.1mol/LB1µ»Ãª˝ªÏ∫œ∫ۻݓ∫÷–¿Î◊”≈®∂»¥Û–°πÿœµŒ™ °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒŞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com