
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)

| OH- | NO3- | Cl- | SO42- | CO32- | |
| H+ | ШмЁЂЛг | ШмЁЂЛг | Шм | ШмЁЂЛг | |
| Na+ | Шм | Шм | Шм | Шм | Шм |
| Ca+ | ЮЂ | Шм | Шм | ЮЂ | ВЛ |
| Ba2+ | Шм | Шм | Шм | ВЛ | ВЛ |
| Cu2+ | ВЛ | Шм | Шм | Шм | ВЛ |
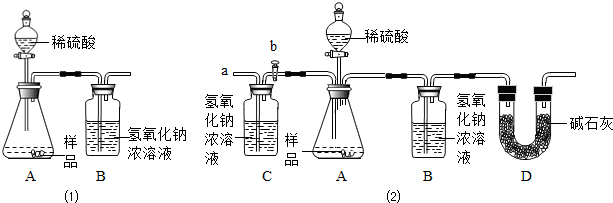
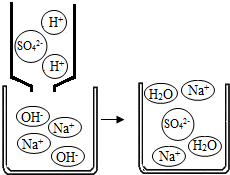 ЃЈ2013?НЈкўЧјвЛФЃЃЉЧтбѕЛЏФЦЫзУћПСадФЦЃЌЪЧвЛжжживЊЕФЛЏЙЄдСЯЃЎЯТСабаОПДгЦфНсЙЙЁЂжЦБИЗНЗЈЁЂаджЪвдМАБфЛЏЙцТЩЕШНЧЖШНјааЃЌЧыИљОнвЊЧѓЛиД№ЯргІЮЪЬтЃЎ
ЃЈ2013?НЈкўЧјвЛФЃЃЉЧтбѕЛЏФЦЫзУћПСадФЦЃЌЪЧвЛжжживЊЕФЛЏЙЄдСЯЃЎЯТСабаОПДгЦфНсЙЙЁЂжЦБИЗНЗЈЁЂаджЪвдМАБфЛЏЙцТЩЕШНЧЖШНјааЃЌЧыИљОнвЊЧѓЛиД№ЯргІЮЪЬтЃЎ| ЪЕбщВНжш | ЪЕбщЯжЯѓ |
| ЂйШЁЩйСПАзЩЋЙЬЬхгкЪдЙмжаЃЌМгЫЎеёЕДКѓЃЌжСШЋВПШмНт | ЮоЩЋШмвК |
| ЂкЯђЪдЙмЕФШмвКжаЕЮМгЪЪСПЮяжЪXЕФШмвК | ЯжЯѓA |
| ЂлдйЯђЪдЙмжаЕЮМгМИЕЮЗгЬЊЪдвКЃЎ | ЯжЯѓB |
| NaHCO3 | Na2CO3 | |
| МгШыЯЁбЮЫс | ЯжЯѓЂё | ВњЩњЦјХн |
| МгШыБЅКЭЪЏЛвЫЎ | ШмвКБфЛызЧ | ЯжЯѓЂђ |
| МгШыCaCl2ШмвК | ЮоУїЯдЯжЯѓ | ШмвКБфЛызЧ |
| МгШШШмвКжСЗаЬкЃЌНЋЦјЬхЭЈШыГЮЧхЪЏЛвЫЎ | ГЮЧхЪЏЛвЫЎБфЛызЧ | ГЮЧхЪЏЛвЫЎЮоУїЯдБфЛЏ |
| ЪЕбщВНжш | ЪЕбщЯжЯѓ | |
| ЂйШЁЩйСПбљЦЗШмгкЫЎЃЌМгШыЙ§СПЕФCaCl2ШмвКЃЎ | гаАзЩЋГСЕэВњЩњ гаАзЩЋГСЕэВњЩњ ЃЛ |
ИУЗДгІЕФЗНГЬЪНЃК Na2CO3+CaCl2ЈTCaCO3Ё§+2NaCl Na2CO3+CaCl2ЈTCaCO3Ё§+2NaCl ЃЎ |
| ЂкНЋЩЯЪіЗДгІКѓЕФЛьКЯвКЙ§ТЫЃЌШЁТЫвК ЕЮМгЯЁбЮЫс ЕЮМгЯЁбЮЫс ЃЎ |
гаЦјХнУАГі гаЦјХнУАГі ЃЛ |
жЄУїВТЯыЂкГЩСЂЃЎ |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com