
题目列表(包括答案和解析)
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
回答:
(1)乙、丁中溶质的分子式:乙 ,丁
(2)第④步操作中用稀H2SO4浸洗的目的是 (填写字母编号)
a除去未反应的NO3-- b除去未反应的I- c除去未反应的Fe d 除去碱性物质
(3)第⑦步操作可供提纯的方法是 (不要求写具体步骤)。
(4)实验室检验I2 的方法是
(5)甲物质见光易变黑,其原因是(用化学方程式表示)
(6)上述工艺流程中可以得到的副产品主要有 。可以循环利用的物质是 。
(7)写出步骤⑥的离子反应方程式 。
写出步骤⑤的化学方程式 。
(6)有人认为,此工艺流程没有必须搞得这样复杂,只要在富碘卤水中直接通入适量Cl2,再进行第⑦步的实验操作即可,你这样看待这个观点。
(7)物质的分离和提纯有许多方法,通常是根据样品的性质和状态来确定的,结合所学知识,填写下表:
样品的性质和状态 | 实验方法的选择 |
固体样品 |
|
液体样品 |
|
胶体样品 |
|
气体样品 |
|
| c(C) |
| c(A)?c(B) |
| c(C) |
| c(A)?c(B) |
| 1 |
| 3 |
| 1 |
| 30 |
| 1 |
| 30 |
(16分)平衡指的是两个相反方向的变化最后所处的运动状态;在平衡时,两种变化仍在继续进行,但是它们的速率相等;根据变化的性质可分为物理平衡和化学平衡,中学阶段涉及的平衡有气体可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀-溶解平衡等等。
(1)现有容积为1 L的恒温恒容密闭容器,向其中加入2 mol A气体和2 mol B气体后发生如下反应:
A(g) + B(g)  C(g) △H=
- a kJ·mol-1
C(g) △H=
- a kJ·mol-1
20s后,反应达到平衡状态,生成1 mol C气体,放出热量Q1kJ。回答下列问题。
①计算20s内B气体的平均化学反应速率为___________,写出该反应的平衡常数表达式___________。
②保持容器温度和容积不变,若改为向其中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1 与Q2的相互关系正确的是____________(填字母)。
(A)Q1 + Q2 = a (B) Q1 + 2Q2 < 2a (C)Q1 + 2Q2 > 2a (D)Q1 + Q2 < a
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入b mol A气体(b>0)时,v(正)_____v(逆)(填“>”、“<”或“=”),重新达平衡后,C气体的平衡体积分数 (C)
=
(C)
= 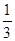 ,则b
= ____________。
,则b
= ____________。
(2)常温下,将VmL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中,充分反应。回答下列问题。(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值_____20.00(填“>”、“<”或“=”),而溶液中c(Na+)、c(CH3COO-)、 c(H+)、c(OH-)的大小关系为_____________________________________________。
②如果V=40.00,则此时溶液中c(OH-) - c(H+) - c(CH3COOH)= ___________________mol·L-1。
实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
|
编号 |
A |
B |
C |
|
发 生 装 置 |
|
|
|
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是 (写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是 (写编号),写出微热时的反应方程式 ;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 ↑ +
8H2O
2KCl + 2MnCl2 + 5Cl2 ↑ +
8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中 元素被氧化, 是氧化剂。当有1mol电子转移时,可生成气体 升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示:

写出圆底烧瓶中发生反应的化学方程式_
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.
(11分)实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。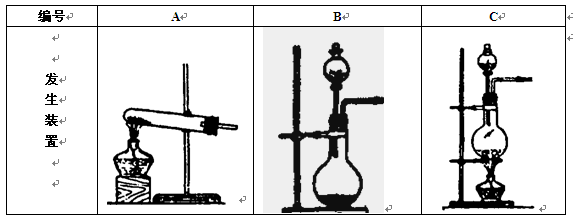
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是 (写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是 (写编号),写出微热时的反应方程式 ;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl  2KCl + 2MnCl2 + 5Cl2
2KCl + 2MnCl2 + 5Cl2  + 8H2O
+ 8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中 元素被氧化, 是氧化剂。当有1mol电子转移时,可生成气体 升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示: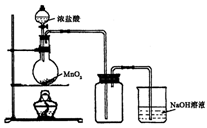
①写出圆底烧瓶中发生反应的化学方程式_
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com