
题目列表(包括答案和解析)
(10分)中学化学中几种常见物质的转化关系如下:(提示:A单质有可变价态且与硫反应生成低价态)
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围:________。
(2)B的化学式:________。
(3)写出:D的溶液与氨水反应的离子方程式:
________________________________________________________________________;
C的溶液与双氧水反应的离子方程式:
________________________________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:
________________________________________________________________________。
(10分)中学化学中几种常见物质的转化关系如下:(提示:A单质有可变价态且与硫反应生成低价态)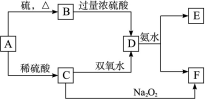
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围:________。
(2)B的化学式:________。
(3)写出:D的溶液与氨水反应的离子方程式:
________________________________________________________________________;
C的溶液与双氧水反应的离子方程式:
________________________________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:
________________________________________________________________________。
(10分)中学化学中几种常见物质的转化关系如下:(提示:A单质有可变价态且与硫反应生成低价态)
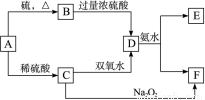
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围:________。
(2)B的化学式:________。
(3)写出:D的溶液与氨水反应的离子方程式:
________________________________________________________________________;
C的溶液与双氧水反应的离子方程式:
________________________________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:
________________________________________________________________________。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com