
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
| |||||||||||||||||||||||||||||||||
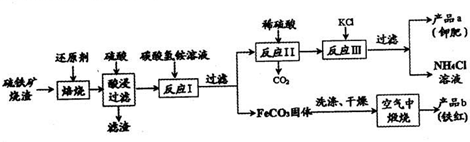
СђЬњПѓЩедќЃЈжївЊГЩЗжЮЊ Fe2O3ЁЂFe3O4ЁЂFeOЁЂSiO2ЕШЃЉЪЧЩњВњСђЫсЕФЙЄвЕЗЯдќЃЌЦфзлКЯРћгУЖдЛЗОГБЃЛЄОпгаЯжЪЕвтвхЁЃРћгУСђЬњПѓЩедќжЦБИЬњКьЕШВњЦЗЕФЪЕбщСїГЬШчЯТЃК

вбжЊМИжжбЮЕФШмНтЖШЫцЮТЖШБфЛЏЕФ
ЧњЯпШчгвЭМЫљЪОЃК

ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЫсНўЁЂЙ§ТЫКѓТЫвКжаЕФН№ЪєбєРызгЪЧ________________ЁЃ
ЃЈ2ЃЉьбЩе FeCO3ЩњГЩВњЦЗ IЕФЛЏбЇЗДгІЗНГЬЪНЮЊ _______ЁЃ
ЪЕбщЪвНјааьбЩеВйзїЫљашвЧ
ЦїГ§СЫОЦОЋХчЕЦЁЂФрШ§НЧЁЂШ§НХМмЁЂВЃСЇАєЭтЃЌЛЙга__________ЁЃ
ЃЈ3ЃЉВњЦЗЂђЕФЛЏбЇЪНЮЊ _______________ЃЌЮЊСЫЛёЕУВњЦЗЂђЃЌЯђ ЃЈNH4ЃЉ2SO4ШмвКжаМгШыKClШмвККѓЃЌЛЙашвЊНјааЕФВйзїЪЧЃКЁЃ
ЃЈ4ЃЉМьбщВњЦЗ IIжаЪЧЗёКЌгаТШЛЏЮядгжЪЕФЪЕбщВйзїЪЧЃКШЁЩйСПВњЦЗЂђгкЪдЙмжаХфГЩШмвКЃЌ ЁЃ
СђЬњПѓЩедќЃЈжївЊГЩЗжЮЊ Fe2O3ЁЂFe3O4ЁЂFeOЁЂSiO2ЕШЃЉЪЧЩњВњСђЫсЕФЙЄвЕЗЯдќЃЌЦфзлКЯРћгУЖдЛЗОГБЃЛЄОпгаЯжЪЕвтвхЁЃРћгУСђЬњПѓЩедќжЦБИЬњКьЕШВњЦЗЕФЪЕбщСїГЬШчЯТЃК

вбжЊМИжжбЮЕФШмНтЖШЫцЮТЖШБфЛЏЕФ
ЧњЯпШчгвЭМЫљЪОЃК
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЫсНўЁЂЙ§ТЫКѓТЫвКжаЕФН№ЪєбєРызгЪЧ________________ЁЃ
ЃЈ2ЃЉьбЩе FeCO3ЩњГЩВњЦЗ IЕФЛЏбЇЗДгІЗНГЬЪНЮЊ _______ЁЃ
ЪЕбщЪвНјааьбЩеВйзїЫљашвЧ
ЦїГ§СЫОЦОЋХчЕЦЁЂФрШ§НЧЁЂШ§НХМмЁЂВЃСЇАєЭтЃЌЛЙга__________ЁЃ
ЃЈ3ЃЉВњЦЗЂђЕФЛЏбЇЪНЮЊ _______________ЃЌЮЊСЫЛёЕУВњЦЗЂђЃЌЯђЃЈNH4ЃЉ2SO4ШмвКжаМгШыKClШмвККѓЃЌЛЙашвЊНјааЕФВйзїЪЧЃКЁЃ
ЃЈ4ЃЉМьбщВњЦЗ IIжаЪЧЗёКЌгаТШЛЏЮядгжЪЕФЪЕбщВйзїЪЧЃКШЁЩйСПВњЦЗЂђгкЪдЙмжаХфГЩШмвКЃЌ ЁЃ
СђЬњПѓЩедќЃЈжївЊГЩЗжЮЊ Fe2O3ЁЂFe3O4ЁЂFeOЁЂSiO2ЕШЃЉЪЧЩњВњСђЫсЕФЙЄвЕЗЯдќЃЌЦфзлКЯРћгУЖдЛЗОГБЃЛЄОпгаЯжЪЕвтвхЁЃРћгУСђЬњПѓЩедќжЦБИЬњКьЕШВњЦЗЕФЪЕбщСїГЬШчЯТЃК
вбжЊМИжжбЮЕФШмНтЖШЫцЮТЖШБфЛЏЕФ
ЧњЯпШчгвЭМЫљЪОЃК
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЫсНўЁЂЙ§ТЫКѓТЫвКжаЕФН№ЪєбєРызгЪЧ________________ЁЃ
ЃЈ2ЃЉьбЩе FeCO3ЩњГЩВњЦЗ IЕФЛЏбЇЗДгІЗНГЬЪНЮЊ _______ЁЃ
ЪЕбщЪвНјааьбЩеВйзїЫљашвЧ
ЦїГ§СЫОЦОЋХчЕЦЁЂФрШ§НЧЁЂШ§НХМмЁЂВЃСЇАєЭтЃЌЛЙга__________ЁЃ
ЃЈ3ЃЉВњЦЗЂђЕФЛЏбЇЪНЮЊ _______________ЃЌЮЊСЫЛёЕУВњЦЗЂђЃЌЯђ ЃЈNH4ЃЉ 2SO4ШмвКжаМгШыKClШмвККѓЃЌЛЙашвЊНјааЕФВйзїЪЧЃКЁЃ
2SO4ШмвКжаМгШыKClШмвККѓЃЌЛЙашвЊНјааЕФВйзїЪЧЃКЁЃ
ЃЈ4ЃЉМьбщВњЦЗ IIжаЪЧЗёКЌгаТШЛЏЮядгжЪЕФЪЕбщВйзїЪЧЃКШЁЩйСПВњЦЗЂђгкЪдЙмжаХфГЩШмвКЃЌ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com