(2012?唐山三模)下图是元素周期的一部分,按要求回答下列问题.

(1)Fe在元素周期表中位于
四
四
周期,
VIII
VIII
族.
(2)写出由元素①、⑥形成的既含极性键又含非极键的化合物的结构式
H-O-O-H
H-O-O-H
;M是由⑦、⑧元素形成的四原子分子,其各元素原子的最外层电子数满足8电子稳定结构,写出M的电子式
.
(3)A、B、C、D、E、X是由上表给出的元素组成的单质或化合物,存在如下转化关系(部分生成物和反应条件已略去).

若E为氧化物,X为单质,则A与水反应的离子方程式为
3NO2+H2O=2H++2NO3-+NO
3NO2+H2O=2H++2NO3-+NO
,写出由B生成C的化学方程式
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
,当生成D的物质的量为0.3mol时,理伦上至少消耗A
1.2
1.2
mol.
(4)以葡萄糖为燃料的微生物燃料电池结构示意图如下,写出该电池的负极反应
C6H12O6+6H2O-24e-=6CO2+24H+
C6H12O6+6H2O-24e-=6CO2+24H+

.


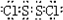
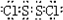

 .
.
 下图所示(反应条件均已略去).
下图所示(反应条件均已略去).