
题目列表(包括答案和解析)
图1-5-17是实验室制备TiCl4的反应装置,主要操作步骤为:
①连接好整套装置,在通Cl2前先通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。

图1-5-17
试完成下列各题:
(1)正确的操作顺序为(填序号)_______________________________________________。
(2)装置A中的反应的离子方程式为__________________________________________。
(3)操作①的目的是_________________________________________________________。
(4)装置D中冷凝管进水口的位置是________(填a或b),装置E的作用是________________
____________________________________________________________________。
(5)TiCl4露置于空气中极易水解,其化学方程式可表示为_________________________。
(6)工业上常用金属镁在800℃和氩气氛围中还原TiCl4的方法制备钛,TiCl4+2Mg![]()
Ti+2MgCl2,氩气的作用为___________________________________________。
图11-2是实验室模拟工业生产制备四氯化钛的反应装置,其主要操作步骤有:①连接好整套装置,在通Cl2前先通入干燥的CO2气体并持续一段时间;②当锥形瓶中的TiCl4的量不再增加时,停止加热,改通CO2气体直至电炉中的瓷管冷却为止;③将TiO2、炭粉混合均匀后,装入管式电炉中;④将电炉升温至800 ℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。 ?
?
图11-2
试完成下列问题:?
(1)正确的操作程序是(填写操作步骤的序号) 。?
(2)装置A中的化学反应方程式为 。?
(3)操作①的目的是 。?
(4)装置D中冷凝管进水口的位置是(填“a”或“b”),装置E的作用是 。
(5)少量TiCl4露置于空气中,可看到的现象是 ,其化学方程式可表示为 。
(6)钛被誉为“21世纪的金属”,在工农业生产、医疗、国防、科技等方面中有着极其广泛而重要的用途。工业上,常用金属镁在800 ℃高温和氩气氛围中还原TiCl4的方法制备钛,试写出该反应的化学方程式 。
四氯化钛(TiCl4)是工业上制备金属钛的重要原料。常温下,它是一种极易水解的无色液体,沸点为136.4℃。工业制备TiCl4和钛的反应分别为:
TiO2 +2C+2Cl2![]() TiCl4 +2CO ;TiCl4 +2Mg
TiCl4 +2CO ;TiCl4 +2Mg ![]() Ti + 2MgCl2
Ti + 2MgCl2
下图是实验室制备TiCl4的反应装置,主要操作步骤:

①连接好整套装置,在通Cl2前先从侧管中通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④ 将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。
试回答下列问题:
⑴ 正确的操作顺序为(填序号)___________________________ 。
⑵ 装置A中反应的离子方程式为__________________________________ 。
⑶ 装置D中冷凝管进水口的位置是(填a或b)___ 。
⑷ TiCl4露置于空气中极易水解,其化学方程式可表示为_____________________ 。
⑸ 工业上常用金属镁在800℃高温和氩气氛围中还原TiCl4的方法制备钛,氩气的作用为__ 。
四氯化钛(TiCl4)是工业上制备金属钛的重要原料。常温下,它是一种极易水解的无色液体,沸点为136.4℃。工业制备TiCl4和钛的反应分布为:
TiO2 +2C+2Cl2![]() TiCl4 +2CO ;TiCl4 +2Mg
TiCl4 +2CO ;TiCl4 +2Mg Ti + 2MgCl2
下图是实验室制备TiCl4的反应装置,主要操作步骤:
①连接好整套装置,在通Cl2前先通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④ 将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。
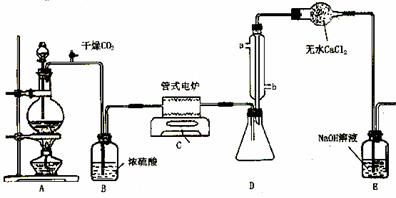
试回答下列问题:
⑴.正确的操作顺序为(填序号)___________________________。
⑵.装置A中的反应的离子方程式为__________________________。
⑶.操作①的目的是_________________________________。
⑷.装置D中冷凝管进水口的位置是(填a或b)_________,
装置E的作用是___________________________________________________。
⑸.TiCl4露置于空气中极易水解,其化学方程式可表示为_____________________。
⑹.工业上常用金属镁在800℃高温和氩气氛围中还原TiCl4的方法制备钛,
![]() ,氩气的作用为_____________________________.
,氩气的作用为_____________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com