
题目列表(包括答案和解析)
试回答下列问题:
(1)下列实验中所选用的仪器或操作以及结论不合理的是___ _。
A.用托盘天平称量11.7g 氯化钠晶体
B.加热NH4Cl晶体时,用湿润红色石蕊试纸靠近试管口,检验NH3的生成
C.不宜用瓷坩埚灼烧氢氧化钠、碳酸钠
D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水湿润过的pH试纸上与标准比色卡比较
E.仅用蒸馏水和pH试纸,就可以鉴别pH相等的H2SO4和CH3COOH溶液
F.用锌和稀硫酸制H2时,为了使制取H2的速率加快,可以向稀硫酸溶液中加入少量CuSO4溶液
G.用碱式滴定管量取20.00mL 0.1000mol/L的KMnO4溶液;
H.不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
I.用瓷坩埚高温熔融![]() 和
和![]() 固体混合物;
固体混合物;
J.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备![]() 胶体;
胶体;
K.配制![]() 饱和溶液时,加入少量的稀硫酸.
饱和溶液时,加入少量的稀硫酸.
(2)欲量取20.00mL Na2CO3溶液,应选用的仪器是 。
(3)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(4)在硫酸铜晶体中结晶水含量的测定实验中,称量操作至少要进行 次。
| A.用托盘天平称量11.7g氯化钠晶体 |
| B.加热NH4Cl晶体时,用湿润红色石蕊试纸靠近试管口,检验NH3的生成 |
| C.不宜用瓷坩埚灼烧氢氧化钠、碳酸钠 |
| D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水湿润过的pH试纸上与标准比色卡比较 |
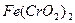 和
和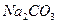 固体混合物;
固体混合物;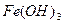 胶体;
胶体;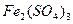 饱和溶液时,加入少量的稀硫酸.
饱和溶液时,加入少量的稀硫酸.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com