
题目列表(包括答案和解析)
下列叙述中正确的是( )
A.标准状况下,2.24L CHCl3含有的分子数为0.1NA
B.1.8 g 的NH4+ 离子中含有的电子数为NA
C.常温常压下,48g O3 含有的氧原子数为NA
D.0.1mol CnH2n+2中含有的碳碳单键数为0.1n NA
下列叙述中正确的是
A.能发生酯化反应的酸一定是羧酸
B.油脂的水解反应又叫皂化反应
C.天然蛋白质水解的最后产物是多种 -氨基酸
-氨基酸
D.淀粉、纤维素、油脂都是高分子化合物
下列叙述中正确的是
A、在碱金属元素中,所有碱金属的氧化物均属于碱性氧化物
B、由于活泼性Na<K,故金属钾可以从NaCl溶液中置换出钠单质
C、碱金属在自然界中都以游离态存在.
D、虽然自然界含钾的物质均易溶于水,但土壤中钾含量太少,故需施用钾肥
合成氨反应工艺成为人工固氮的最重要途径。N2(g)+3H2(g)
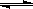 2 NH3 (g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中正确的是
2 NH3 (g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中正确的是
A. 正反应速率增大,逆反应速率减小,平衡一定向正反应方向移动
B. 正反应速率减小,逆反应速率减小,平衡一定向逆反应方向移动
C. 若同时扩大容器的体积,则正逆反应速率一定都减小,平衡向逆反应方向移动
D. 若温度降低至氨气液化,则平衡一定向正反应方向移动,氨气产率提高
已知:N2(g)+3H2(g)  2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ。已知Q2=3Q1,下列叙述中正确的是 :
2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ。已知Q2=3Q1,下列叙述中正确的是 :
A.平衡时甲容器中NH3(g)的体积分数比乙容器中的小
B.平衡时甲容器中气体的压强为开始时压强的
C.达到平衡时,甲容器中H2的转化率为25%
D.Q1=Q
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com