
题目列表(包括答案和解析)
| A、将等质量硫蒸气和硫粉分别完全燃烧,前者放出热量多 | B、由“C(石墨)=C(金刚石);△H=+l.9 kJ?mol-1”可知金刚石比石墨稳定 | C、稀的强酸和稀的强碱溶液反应的热化学方程式均为:H++OH-=H2O(l);△H=-57.3 kJ?mol-1 | D、在25℃、101 kPa时.1克氢气完全燃烧生成H2O放出热量142.9 kJ.则:2H2O(l)=2H2(g)+O2(g);△H=+285.8 kJ?mol-1 |
 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:| 1 |
| 2 |
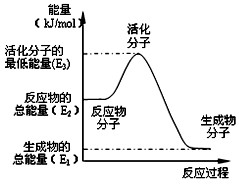
| A、反应②中的能量变化如图所示,则△H2=E1-E3 |
| B、CH3OH的燃烧热△H=-192.9 kJ?mol -1 |
| C、H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收能量 |
| D、根据②推知:在25℃,101 kPa时,1mol CH3OH(g)燃烧生成CO2和H2O(l)放出的热量应大于192.9 kJ |
在25 ℃、101 kPa下,1 g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68 kJ。下列热化学方程式正确的是( )
A.CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(l) ΔH=+725.8 kJ·mol-1
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
C.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-725.8 kJ·mol-1
D.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=+1452 kJ·mol-1
在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+![]() O2(g)====CO2(g)+2H2O(l);ΔH=+725.8 kJ·mol-1
O2(g)====CO2(g)+2H2O(l);ΔH=+725.8 kJ·mol-1
B.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l);ΔH=-1 452 kJ·mol-1
C.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l);ΔH=-725.8 kJ·mol-1
D.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l);ΔH=+1 452 kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com