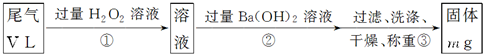ЃЈ2013?ГЄЩГФЃФтЃЉСђЫсЙЄвЕЮВЦјжаЖўбѕЛЏСђЕФКЌСПГЌЙ§0.05%ЃЈЬхЛ§ЗжЪ§ЃЉЪБашОДІРэКѓВХФмХХЗХЃЎФГаЃЛЏбЇаЫШЄаЁзщгћВтЖЈФГСђЫсЙЄГЇХХЗХЮВЦјжаЖўбѕЛЏСђЕФКЌСПЃЌЗжБ№ВЩгУвдЯТЗНАИЃК
ЁОМзЗНАИЁПШчЭМЫљЪОЃЌЭМжаЦјЬхСїСПМЦBгУгкзМШЗВтСПЭЈЙ§ЕФЮВЦјЬхЛ§ЃЎНЋЮВЦјЭЈШывЛЖЈЬхЛ§вбжЊХЈЖШЕФЕтЫЎжаВтЖЈSO
2ЕФКЌСПЃЎЕБЯДЦјЦПCжаШмвКРЖЩЋЯћЪЇЪБЃЌСЂМДЙиБеЛюШћAЃЎ
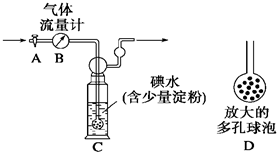
ЃЈ1ЃЉЯДЦјЦПCжаЕМЙмФЉЖЫСЌНгвЛИіЖрПзЧђХнDЃЌПЩвдЬсИпЪЕбщЕФзМШЗЖШЃЌЦфРэгЩЪЧ
діДѓSO2гыЕтЫЎЕФНгДЅУцЛ§ЃЌЪЙSO2КЭЕтЫЎГфЗжЗДгІ
діДѓSO2гыЕтЫЎЕФНгДЅУцЛ§ЃЌЪЙSO2КЭЕтЫЎГфЗжЗДгІ
ЃЎ
ЃЈ2ЃЉЯДЦјЦПCжаШмвКРЖЩЋЯћЪЇКѓЃЌУЛгаМАЪБЙиБеЛюШћAЃЌВтЕУЕФSO
2КЌСП
ЦЋЕЭ
ЦЋЕЭ
ЃЈЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБЃЉЃЎ
ЁОввЗНАИЁПЪЕбщВНжшШчЯТУцСїГЬЭМЫљЪОЃК
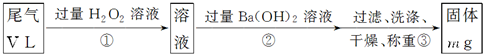
ЃЈ3ЃЉВНжшЂйжаЙ§СПH
2O
2ЕФзїгУЪЧ
НЋSO2ЭъШЋзЊЛЏЮЊSO42-
НЋSO2ЭъШЋзЊЛЏЮЊSO42-
ЃЛ
ЃЈ4ЃЉаДГіВНжшЂкжаЗДгІЕФЛЏбЇЗНГЬЪН
H2SO4+BaЃЈOHЃЉ2=BaSO4Ё§+2H2O
H2SO4+BaЃЈOHЃЉ2=BaSO4Ё§+2H2O
ЃЛ
ЃЈ5ЃЉВНжшЂкжаBaЃЈOHЃЉ
2ЪЧЗёзуСПЕФХаЖЯЗНЗЈЪЧ
ОВжУЗжВуКѓЃЌЯђЩЯВуЧхвКжаМЬајЕЮМгBaЃЈOHЃЉ2ШмвКЃЌШєЮоЛызЧЯжЯѓВњЩњЫЕУїBaЃЈOHЃЉ2зуСПЃЌЗёдђВЛзу
ОВжУЗжВуКѓЃЌЯђЩЯВуЧхвКжаМЬајЕЮМгBaЃЈOHЃЉ2ШмвКЃЌШєЮоЛызЧЯжЯѓВњЩњЫЕУїBaЃЈOHЃЉ2зуСПЃЌЗёдђВЛзу
ЃЎ
ЃЈ6ЃЉЭЈЙ§ЕФЮВЦјЬхЛ§ЮЊV LЃЈвбЛЛЫуГЩБъзМзДПіЃЉЪБЃЌИУЮВЦјжаЖўбѕЛЏСђЕФКЌСПЃЈЬхЛ§ЗжЪ§ЃЉЮЊ
ЃЈгУКЌгаVЁЂmЕФДњЪ§ЪНБэЪОЃЉЃЎ