二甲醚(CH
3OCH
3)被称为21世纪的新型能源,是一种高效、清洁能源.
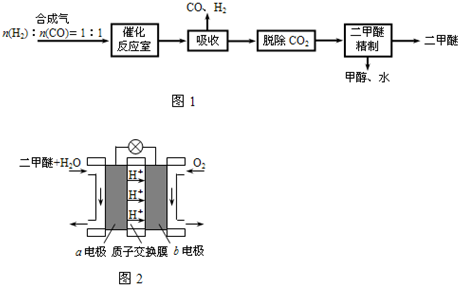
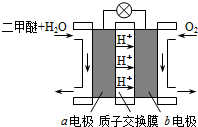
Ⅰ.工业制备二甲醚的生产流程如下:

催化反应室中(压力2.0~10.0Mpa,温度230~280℃)发生如下反应:
①CO(g)+2H
2(g)?CH
3OH(g)△H=-90.7kJ/mol
②2CH
3OH(g)?CH
3OCH
3(g)+H
2O(g)△H=-23.5kJ/mol
③CO(g)+H
2O(g)?CO
2(g)+H
2(g)△H=-41.2kJ/mol
(1)二甲醚也可以通过天然气和CO
2合成制得,该反应的化学方程式为
3CH4+CO2→2CH3OCH3
3CH4+CO2→2CH3OCH3
.
(2)催化反应室中总反应3CO(g)+3H
2(g)?CH
3OCH
3(g)+CO
2(g)的△H=
-246.1kJ/mol
-246.1kJ/mol
,830℃时反应③的K=1.0,则在催化反应室中反应③的K
>
>
1.0(填“>”、“<”或“=”).
(3)在温度相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒压,发生反应②,测得反应达到平衡时的有关数据如下.
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
1mol CH3OCH3、1mol H2O |
2mol CH3OH |
1mol CH3OH |
| CH3OH的浓度(mol/L) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
吸收a kJ |
放出b kJ |
放出c kJ |
| 平衡时体积(L) |
V1 |
V2 |
V3 |
| 反应物转化率 |
α 1 |
α 2 |
α 3 |
下列说法正确的是
A、B、C
A、B、C
.(填字母序号)
A.a+2c=23.5 B.α
1+α
2=1 C.V
1>V
3 D.c
1=2c
3(4)上述生产流程中,可以循环使用的物质有
甲醇和水、CO和H2
甲醇和水、CO和H2
.
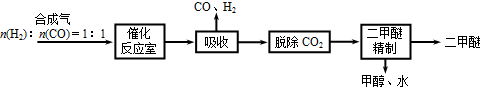
Ⅱ.用二甲醚-空气碱性(KOH)燃料电池作电源电解精炼粗铜(如图),在接通电路一段时间纯Cu质量增加3.2g.

(5)请写出燃料电池中的负极反应式:
CH3OCH3-12e-+16OH-=2CO32-+11H2O
CH3OCH3-12e-+16OH-=2CO32-+11H2O
.
(6)燃料电池正极消耗标准状况下空气的体积是
2.8L
2.8L
(空气中O
2体积分数以20%计算).