
题目列表(包括答案和解析)

| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 5.7 |
| 完全沉淀pH | 3.7 | 9.6 | 8.0 |
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
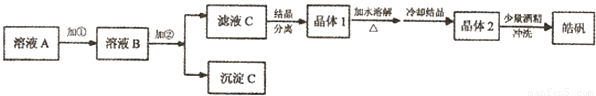
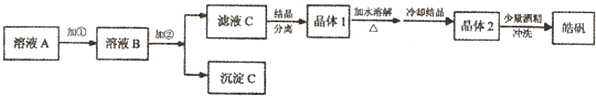
用粗锌(含少量Fe等杂质)与稀硫酸反应制氢气时,其废液中含有大量的硫酸锌。同学们用该废液来制取皓矾(ZnSO4·7H2O)。 制备皓矾的实验流程如下图所示:
![]()

![]()
![]() 已知:氢氧化物沉淀的pH范围见下表。
已知:氢氧化物沉淀的pH范围见下表。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
开始沉淀pH | 2.7 | 7.6 | 5.7 |
完全沉淀pH | 3.7 | 9.6 | 8.0 |
![]() 请回答下列问题:
请回答下列问题:
![]() (1)供选择的试剂a有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,应选用 ,其理由是 。
(1)供选择的试剂a有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,应选用 ,其理由是 。
![]() (2) 供选择的试剂b有: Zn粉、ZnO、Zn(OH)2、ZnCO3、ZnSO4等,应选用 ,其理由是 。
(2) 供选择的试剂b有: Zn粉、ZnO、Zn(OH)2、ZnCO3、ZnSO4等,应选用 ,其理由是 。
![]() (3)晶体l→晶体2,该操作的名称是 。
(3)晶体l→晶体2,该操作的名称是 。
![]() (4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是 。
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是 。
![]()

| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com