
题目列表(包括答案和解析)
1 g CuO和木炭粉的混合物,在隔绝空气的条件下加热一段时间并冷却,质量变为 x g,
若反应中只产生CO2。
(1)实验中有 g CuO被还原, (2)x的取值范围是 。
1 g CuO和木炭粉的混合物,在隔绝空气的条件下加热一段时间并冷却,质量变为 x g,
若反应中只产生CO2。
(1)实验中有 g CuO被还原, (2)x的取值范围是 。
1 g CuO和木炭粉的混合物,在隔绝空气的条件下加热一段时间并冷却,质量变为 x g,
若反应中只产生CO2。
(1)实验中有 g CuO被还原, (2)x的取值范围是 。
1 g CuO和木炭粉的混合物,在隔绝空气的条件下加热一段时间并冷却,质量变为 x g,
若反应中只产生CO2。
(1)实验中有 g CuO被还原, (2)x的取值范围是 。
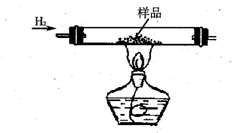 实验室有CuO和铜粉的混合物.要测定该样品(已称得其质量为m g)中氧化铜的质量分数.
实验室有CuO和铜粉的混合物.要测定该样品(已称得其质量为m g)中氧化铜的质量分数.| 实验方法 | 有关化学方程式 | 实验用仪器(填序号) | 实验需直接测定的物理量(用文字说明) |
| (1) | H2SO4+CuO═CuSO4+H2O | ||
| (2) | 实验前坩埚与样品总质量(或坩埚质量)、实验后坩埚与CuO总质量 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com