
题目列表(包括答案和解析)
通过海水晾晒可得粗盐。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示。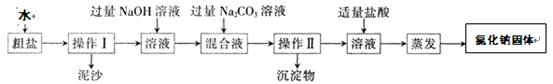
根据以上信息回答:
(1)操作Ⅰ和操作Ⅱ的名称是 。该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 (填序号)。 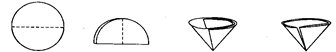
A B C D
(2)蒸发容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取 等措施。
(3)在实验过程中加入过量的NaOH溶液的目的是 。
(4)判断加入的盐酸“适量”的方法是 。
(5)实验所得氯化钠固体的质量大于粗盐中NaCl的质量,原因是 。
(6)若用所得氯化钠配制50g质量分数为6%的氯化钠溶液,除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是 ,其作用是 。
通过海水晾晒可得粗盐。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示。
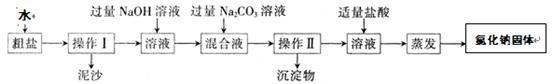
根据以上信息回答:
(1)操作Ⅰ和操作Ⅱ的名称是 。该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 (填序号)。
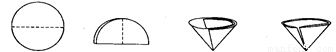
A B C D
(2)蒸发容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取 等措施。
(3)在实验过程中加入过量的NaOH溶液的目的是 。
(4)判断加入的盐酸“适量”的方法是 。
(5)实验所得氯化钠固体的质量大于粗盐中NaCl的质量,原因是 。
(6)若用所得氯化钠配制50g质量分数为6%的氯化钠溶液,除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是 ,其作用是 。


“侯氏制碱法“制得的炖碱(Na2CO3)中常含有少量氯化钠,某化学兴趣小
组的同学拟侧定某纯碱样品中Na2CO3的质量分数。
【方案一】沉淀分析法(如下图所示)

则:
(1)"操作I.的名称是 。
(2)溶液M中含有的阳离子有 。
(3)确定CaCl2溶液是否过量的方法是 。
A 静置混合物,向上层溶液中再滴加CaCl2溶液,如果无沉淀,则过量
B 向落液M中滴加CaCl2溶液,如果有沉淀,则过量
(4)若沉淀A^没有洗涤、烘干,导致Na2CO3的质量分数 (填“偏大”“偏小”“不变”).判断沉淀A洗净的方法是:取最后一次洗涤所得滤液,滴加AgNO3溶液,若 (填“有”或“无”)白色沉淀,则洗涤干净.
(5)样品中Na2CO3的质量分数为 (用字母m ,n的代数式表示)。
【方案二】气体分析法

(1)A装置中反应的化学方程式为 ,盛放稀硫酸的仪器名称为
(2)B装置的作用是 C装置中反应的化学方程式为
(3)通过称 装置中反应前后的质量,即可求得产生二氧化碳的质量。
(4)理论上【方案二】比【方案一】会产生较大的误差,原因是 
在自制的简易净水器中,常加入活性炭,其作用是 ;发生地震、洪涝灾害地区的灾民用以下几个步骤可将已通过自然沉降滤去泥沙的河水转化为饮用水,其处理过程为①加入明矾、②加入漂白粉、③静置沉淀、④加热煮沸。其合理的顺序是(填序号) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com