
题目列表(包括答案和解析)
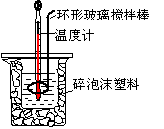
用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。
| | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1) /℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.5 | 24.50 | 27.5 | 3.00 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
用50 mL0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。

|
|
起始温度t1/℃ |
终止温度 t2/℃ |
温度差 (t2-t1) /℃ |
||
|
HCl |
NaOH |
平均值 |
|||
|
1 |
25.5 |
25.0 |
25.25 |
28.5 |
3.25 |
|
2 |
24.5 |
24.5 |
24.50 |
27.5 |
3.00 |
|
3 |
25.0 |
24.5 |
24.75 |
26.5 |
1.75 |
(1)在该实验中,量取50 mL 盐酸或NaOH 溶液,需要用到的玻璃仪器_________。
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指______________________________温度。
(4)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g·℃ )。
(5) 如果用50 mL 0.55mol/L的氨水(NH3·H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是
________________________ 。
| | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差 (t2-t1) /℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.5 | 24.50 | 27.5 | 3.00 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(10分)用50 mL 0.50mol?L-1盐酸与50 mL 0.55 mol?L-1 NaOH溶液,在如图所示 的装置中进行中和反应,测定强酸与强碱反应的反应热。
的装置中进行中和反应,测定强酸与强碱反应的反应热。
| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | ||
|
| 平均值 | |||
1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(1)在该实验中,量取50 mL盐酸或NaOH溶液,需要用到的玻璃仪是 ;
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是 ;
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指 温度;
(4)计算该实验发生中和反应时放出的热量为 kJ[中和后生成的溶液的比热容c=4.18 J?(g?℃)-1,稀溶液的密度都为1 g?cm-3];
(5)如果用50 mL 0.55 mol?L一的氨水(NH3?H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是 。
已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为无色液体.反应生成的水均已略去.它们有如下图所示的关系.

(1)写出化学式:A________ B________ J________.
(2)反应③中每生成1 mol F,转移电子的数目为:________.
(3)反应④的化学方程式为:________.
(4)写出离子方程式分别为:反应②________;⑤________.
(5)反应①中,每1.00 g C与足量的F作用,恢复到25℃放出55.6 kJ热量,写出反应①的热化学方程式 ________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com