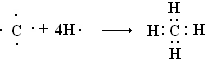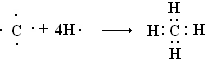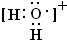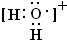∂Ã÷Ð∆⁄÷˜◊‘™ÀÿA°¢B°¢C°¢D°¢Eµƒ‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û£¨À¸√«‘≠◊”∫ÀÕ‚µƒµÁ◊”≤„ ˝÷Æ∫ÕŒ™10£ªB‘™ÀÿµƒªØ∫œŒÔ÷÷¿ý∑±∂ý£¨ ˝ƒø≈”¥Û£ÆC°¢D¡Ω÷÷‘™Àÿ–Œ≥…µƒµ•÷ «ø’∆¯÷–∫¨¡ø◊Ó∂ýµƒŒÔ÷ £ªD°¢E¡Ω‘™Àÿø…“‘…˙≥…¡Ω÷÷≤ªÕ¨µƒ¿Î◊”ªØ∫œŒÔ£Æ
£®1£©”…A°¢C°¢D»˝‘™ÀÿÀ˘–Œ≥…≥£º˚—ŒA
4C
2D
3µƒ»Ð“∫≥
À·
À·
–‘£®ÃÓ°∞À·°±°¢°∞÷–°±°¢°∞ºÓ°±£©£¨∆‰‘≠“Ú”√¿Î◊”∑Ω≥Ã Ω±Ì æŒ™£∫
NH
4++H
2O

NH
3?H
2O+H
+NH
4++H
2O

NH
3?H
2O+H
+£Æ
£®2£©Bµƒœý∂‘∑÷◊”÷ ¡ø◊Ó–°µƒ«‚ªØŒÔµƒ»º…’»»Œ™890.3kJ?mol
-1£¨–¥≥ˆ∆‰»º…’µƒªØ—ß∑Ω≥à Ω
CH4£®g£©+2O2£®g£©®TCO2£®g£©+2H2O£®l£©°˜H=-890.3KJ/mol
CH4£®g£©+2O2£®g£©®TCO2£®g£©+2H2O£®l£©°˜H=-890.3KJ/mol
£Æ
£®3£©X°¢Y «æ˘”…C°¢D¡Ω‘™Àÿ◊È≥…µƒªØ∫œŒÔ£¨«“C°¢D‘⁄X°¢Y÷–µƒº€Ã¨œýÕ¨£¨ƒ≥Œ¬∂»œ¬‘⁄2Lµƒ√б’»ð∆˜÷–X°¢Yœýª•◊™ªØ ±µƒ¡ø±‰πÿœµ»ÁÕº£∫
¢Ÿ∏√∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™
N
2O
4
2NO
2N
2O
4
2NO
2¢⁄∑¥”¶Ω¯––µΩ25min ±£¨∏ƒ±‰µƒÃıº˛ø…ƒÐ «
D
D
A°¢Àı–°»ð∆˜Ãª˝ B°¢≥‰»Î0.4molNO
2C°¢≥‰»Î0.4molN
2O
4 D°¢≥‰»Î0.8molNO
2¢€30min∫Û∑¥”¶‘Ÿ¥Œ¥ÔµΩ∆Ω∫‚£¨¥À ±£¨Y◊™ªØŒ™XµƒªØ—ß∆Ω∫‚≥£ ˝Œ™
0.9
0.9
£®ÃÓ ˝÷µ£©£Æ
¢Ð»Ù∑¥”¶Œ¬∂»≤ª±‰£¨‘⁄2Lµƒ√б’»ð∆˜÷–≥‰»Î1.4molY£¨∑¥”¶¥Ô∆Ω∫‚∫ÛYµƒ◊™ªØ¬ «
£Æ








 ∂Ã÷Ð∆⁄÷˜◊‘™ÀÿA°¢B°¢C°¢D°¢Eµƒ‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û£¨À¸√«‘≠◊”∫ÀÕ‚µƒµÁ◊”≤„ ˝÷Æ∫ÕŒ™10£ªB‘™ÀÿµƒªØ∫œŒÔ÷÷¿ý∑±∂ý£¨ ˝ƒø≈”¥Û£ÆC°¢D¡Ω÷÷‘™Àÿ–Œ≥…µƒµ•÷ «ø’∆¯÷–∫¨¡ø◊Ó∂ýµƒŒÔ÷ £ªD°¢E¡Ω‘™Àÿø…“‘…˙≥…¡Ω÷÷≤ªÕ¨µƒ¿Î◊”ªØ∫œŒÔ£Æ
∂Ã÷Ð∆⁄÷˜◊‘™ÀÿA°¢B°¢C°¢D°¢Eµƒ‘≠◊”–Ú ˝“¿¥Œ‘ˆ¥Û£¨À¸√«‘≠◊”∫ÀÕ‚µƒµÁ◊”≤„ ˝÷Æ∫ÕŒ™10£ªB‘™ÀÿµƒªØ∫œŒÔ÷÷¿ý∑±∂ý£¨ ˝ƒø≈”¥Û£ÆC°¢D¡Ω÷÷‘™Àÿ–Œ≥…µƒµ•÷ «ø’∆¯÷–∫¨¡ø◊Ó∂ýµƒŒÔ÷ £ªD°¢E¡Ω‘™Àÿø…“‘…˙≥…¡Ω÷÷≤ªÕ¨µƒ¿Î◊”ªØ∫œŒÔ£Æ NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+ 2NO2
2NO2 2NO2
2NO2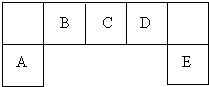 ∂Ã÷Ð∆⁄÷˜◊‘™ÀÿA°¢B°¢C°¢D°¢E‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√»ÁÕº£∫«Îªÿ¥œ¬¡–Œ £∫
∂Ã÷Ð∆⁄÷˜◊‘™ÀÿA°¢B°¢C°¢D°¢E‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√»ÁÕº£∫«Îªÿ¥œ¬¡–Œ £∫