
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
«ΑΥΡ÷ήΤΎ‘ΣΥΊAΓΔBΓΔCΓΔDΓΔEΓΔFΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–AΚΆBΆ§÷ήΤΎΘ§ΙΧΧ§ΒΡAB2Ρή…ΐΜΣΘΜCΚΆE‘≠Ή”ΕΦ”–“ΜΗωΈ¥≥…Ε‘ΒγΉ”Θ§C+±»E-…Ό“ΜΗωΒγΉ”≤ψΘ§E‘≠Ή”ΒΟΒΫ“ΜΗωΒγΉ”Κσ3pΙλΒά»Ϊ≥δ¬ζΘΜDΉνΗΏΦέ―θΜ·Έο÷–DΒΡ÷ ΝΩΖ÷ ΐΈΣ40%Θ§«“ΚΥΡΎ÷ Ή” ΐΒ»”Ύ÷–Ή” ΐΘΜFΈΣΚλ…ΪΒΞ÷ Θ§”–F+ΚΆF2+ΝΫ÷÷άκΉ”ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©‘ΣΥΊΒγΗΚ–‘ΘΚD____E (ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®2Θ©AΓΔCΒΞ÷ »έΒψA_____C(ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®3Θ©AE4÷–A‘≠Ή”‘”Μ·ΙλΒάΖΫ ΫΈΣ:________‘”Μ·ΘΜΤδΙΧΧ§ΨßΧεάύ–ΆΈΣ_______
Θ®4Θ©FΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ______ΘΜœρFΒΡΝρΥα―Έ÷–÷πΒΈΦ”»κΑ±Υ°œ»≤ζ…ζ≥ΝΒμΘ§Κσ≥ΝΒμ»ήΫβΈΣ…νάΕ…Ϊ»ή“ΚΘ§Φ”»κ““¥ΦΜαΈω≥ωάΕ…ΪΨßΧεΘ§ΗΟΨßΧε÷–F”κNH3÷°ΦδΒΡΜ·―ßΦϋΈΣ_______
Θ®5Θ©«βΜ·ΈοΒΡΖ–ΒψΘΚB±»DΗΏΒΡ‘≠“ρ______;
Θ®6Θ©‘ΣΥΊXΒΡΡ≥ΦέΧ§“θάκΉ”Xn-÷–Υυ”–ΒγΉ”’ΐΚΟ≥δ¬ζKΚΆLΒγΉ”≤ψΘ§CnXΨßΧεΒΡΉν–ΓΫαΙΙΒΞ‘Σ»γΆΦΥυ ΨΓΘ

ΗΟΨßΧε÷–―τάκΉ”ΚΆ“θάκΉ”Ηω ΐ±»ΈΣ_______Θ§ΨßΧε÷–ΟΩΗωXn-±Μ_____ΗωΒ»ΨύάκΒΡC+άκΉ”ΑϋΈßΓΘ
«ΑΥΡ÷ήΤΎ‘ΣΥΊAΓΔBΓΔCΓΔDΓΔEΓΔFΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–AΚΆBΆ§÷ήΤΎΘ§ΙΧΧ§ΒΡAB2Ρή…ΐΜΣΘΜCΚΆE‘≠Ή”ΕΦ”–“ΜΗωΈ¥≥…Ε‘ΒγΉ”Θ§C+±»E-…Ό“ΜΗωΒγΉ”≤ψΘ§E‘≠Ή”ΒΟΒΫ“ΜΗωΒγΉ”Κσ3pΙλΒά»Ϊ≥δ¬ζΘΜDΉνΗΏΦέ―θΜ·Έο÷–DΒΡ÷ ΝΩΖ÷ ΐΈΣ40%Θ§«“ΚΥΡΎ÷ Ή” ΐΒ»”Ύ÷–Ή” ΐΘΜFΈΣΚλ…ΪΒΞ÷ Θ§”–F+ΚΆF2+ΝΫ÷÷άκΉ”ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©‘ΣΥΊΒγΗΚ–‘ΘΚD____E (ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®2Θ©AΓΔCΒΞ÷ »έΒψA_____C(ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®3Θ©AE4÷–A‘≠Ή”‘”Μ·ΙλΒάΖΫ ΫΈΣ:________‘”Μ·ΘΜΤδΙΧΧ§ΨßΧεάύ–ΆΈΣ_______
Θ®4Θ©FΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ______ΘΜœρFΒΡΝρΥα―Έ÷–÷πΒΈΦ”»κΑ±Υ°œ»≤ζ…ζ≥ΝΒμΘ§Κσ≥ΝΒμ»ήΫβΈΣ…νάΕ…Ϊ»ή“ΚΘ§Φ”»κ““¥ΦΜαΈω≥ωάΕ…ΪΨßΧεΘ§ΗΟΨßΧε÷–F”κNH3÷°ΦδΒΡΜ·―ßΦϋΈΣ_______
Θ®5Θ©«βΜ·ΈοΒΡΖ–ΒψΘΚB±»DΗΏΒΡ‘≠“ρ______;
Θ®6Θ©‘ΣΥΊXΒΡΡ≥ΦέΧ§“θάκΉ”Xn-÷–Υυ”–ΒγΉ”’ΐΚΟ≥δ¬ζKΚΆLΒγΉ”≤ψΘ§CnXΨßΧεΒΡΉν–ΓΫαΙΙΒΞ‘Σ»γΆΦΥυ ΨΓΘ
ΗΟΨßΧε÷–―τάκΉ”ΚΆ“θάκΉ”Ηω ΐ±»ΈΣ_______Θ§ΨßΧε÷–ΟΩΗωXn-±Μ_____ΗωΒ»ΨύάκΒΡC+άκΉ”ΑϋΈßΓΘ
«ΑΥΡ÷ήΤΎ‘ΣΥΊAΓΔBΓΔCΓΔDΓΔEΓΔFΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–AΚΆBΆ§÷ήΤΎΘ§ΙΧΧ§ΒΡAB2Ρή…ΐΜΣΘΜCΚΆE‘≠Ή”ΕΦ”–“ΜΗωΈ¥≥…Ε‘ΒγΉ”Θ§C+±»E-…Ό“ΜΗωΒγΉ”≤ψΘ§E‘≠Ή”ΒΟΒΫ“ΜΗωΒγΉ”Κσ3pΙλΒά»Ϊ≥δ¬ζΘΜDΉνΗΏΦέ―θΜ·Έο÷–DΒΡ÷ ΝΩΖ÷ ΐΈΣ40%Θ§«“ΚΥΡΎ÷ Ή” ΐΒ»”Ύ÷–Ή” ΐΘΜFΈΣΚλ…ΪΒΞ÷ Θ§”–F+ΚΆF2+ΝΫ÷÷άκΉ”ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©‘ΣΥΊΒγΗΚ–‘ΘΚD____E (ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®2Θ©AΓΔCΒΞ÷ »έΒψA_____C(ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®3Θ©AE4÷–A‘≠Ή”‘”Μ·ΙλΒάΖΫ ΫΈΣ:________‘”Μ·ΘΜΤδΙΧΧ§ΨßΧεάύ–ΆΈΣ_______
Θ®4Θ©FΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ______ΘΜœρFΒΡΝρΥα―Έ÷–÷πΒΈΦ”»κΑ±Υ°œ»≤ζ…ζ≥ΝΒμΘ§Κσ≥ΝΒμ»ήΫβΈΣ…νάΕ…Ϊ»ή“ΚΘ§Φ”»κ““¥ΦΜαΈω≥ωάΕ…ΪΨßΧεΘ§ΗΟΨßΧε÷–F”κNH3÷°ΦδΒΡΜ·―ßΦϋΈΣ_______
Θ®5Θ©«βΜ·ΈοΒΡΖ–ΒψΘΚB±»DΗΏΒΡ‘≠“ρ______;
Θ®6Θ©‘ΣΥΊXΒΡΡ≥ΦέΧ§“θάκΉ”Xn-÷–Υυ”–ΒγΉ”’ΐΚΟ≥δ¬ζKΚΆLΒγΉ”≤ψΘ§CnXΨßΧεΒΡΉν–ΓΫαΙΙΒΞ‘Σ»γΆΦΥυ ΨΓΘ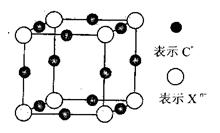
ΗΟΨßΧε÷–―τάκΉ”ΚΆ“θάκΉ”Ηω ΐ±»ΈΣ_______Θ§ΨßΧε÷–ΟΩΗωXn-±Μ_____ΗωΒ»ΨύάκΒΡC+άκΉ”ΑϋΈßΓΘ
«ΑΥΡ÷ήΤΎ‘ΣΥΊAΓΔBΓΔCΓΔDΓΔEΓΔFΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–AΚΆBΆ§÷ήΤΎΘ§ΙΧΧ§ΒΡAB2Ρή…ΐΜΣΘΜCΚΆE‘≠Ή”ΕΦ”–“ΜΗωΈ¥≥…Ε‘ΒγΉ”Θ§C+±»E-…Ό“ΜΗωΒγΉ”≤ψΘ§E‘≠Ή”ΒΟΒΫ“ΜΗωΒγΉ”Κσ3pΙλΒά»Ϊ≥δ¬ζΘΜDΉνΗΏΦέ―θΜ·Έο÷–DΒΡ÷ ΝΩΖ÷ ΐΈΣ40%Θ§«“ΚΥΡΎ÷ Ή” ΐΒ»”Ύ÷–Ή” ΐΘΜFΈΣΚλ…ΪΒΞ÷ Θ§”–F+ΚΆF2+ΝΫ÷÷άκΉ”ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©‘ΣΥΊΒγΗΚ–‘ΘΚD____E (ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®2Θ©AΓΔCΒΞ÷ »έΒψA_____C(ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®3Θ©AE4÷–A‘≠Ή”‘”Μ·ΙλΒάΖΫ ΫΈΣ:________‘”Μ·ΘΜΤδΙΧΧ§ΨßΧεάύ–ΆΈΣ_______
Θ®4Θ©FΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ______ΘΜœρFΒΡΝρΥα―Έ÷–÷πΒΈΦ”»κΑ±Υ°œ»≤ζ…ζ≥ΝΒμΘ§Κσ≥ΝΒμ»ήΫβΈΣ…νάΕ…Ϊ»ή“ΚΘ§Φ”»κ““¥ΦΜαΈω≥ωάΕ…ΪΨßΧεΘ§ΗΟΨßΧε÷–F”κNH3÷°ΦδΒΡΜ·―ßΦϋΈΣ_______
Θ®5Θ©«βΜ·ΈοΒΡΖ–ΒψΘΚB±»DΗΏΒΡ‘≠“ρ______;
Θ®6Θ©‘ΣΥΊXΒΡΡ≥ΦέΧ§“θάκΉ”Xn-÷–Υυ”–ΒγΉ”’ΐΚΟ≥δ¬ζKΚΆLΒγΉ”≤ψΘ§CnXΨßΧεΒΡΉν–ΓΫαΙΙΒΞ‘Σ»γΆΦΥυ ΨΓΘ
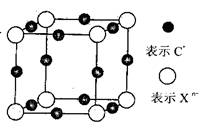
ΗΟΨßΧε÷–―τάκΉ”ΚΆ“θάκΉ”Ηω ΐ±»ΈΣ_______Θ§ΨßΧε÷–ΟΩΗωXn-±Μ_____ΗωΒ»ΨύάκΒΡC+άκΉ”ΑϋΈßΓΘ
«ΑΥΡ÷ήΤΎ‘ΣΥΊAΓΔBΓΔCΓΔDΓΔEΓΔFΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–AΚΆBΆ§÷ήΤΎΘ§ΙΧΧ§ΒΡAB2Ρή…ΐΜΣΘΜCΚΆE‘≠Ή”ΕΦ”–“ΜΗωΈ¥≥…Ε‘ΒγΉ”Θ§C+±»E-…Ό“ΜΗωΒγΉ”≤ψΘ§E‘≠Ή”ΒΟΒΫ“ΜΗωΒγΉ”Κσ3pΙλΒά»Ϊ≥δ¬ζΘΜDΉνΗΏΦέ―θΜ·Έο÷–DΒΡ÷ ΝΩΖ÷ ΐΈΣ40%Θ§«“ΚΥΡΎ÷ Ή” ΐΒ»”Ύ÷–Ή” ΐΘΜFΈΣΚλ…ΪΒΞ÷ Θ§”–F+ΚΆF2+ΝΫ÷÷άκΉ”ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©‘ΣΥΊΒγΗΚ–‘ΘΚD____E (ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®2Θ©AΓΔCΒΞ÷ »έΒψA_____C(ΧνΘΨΓΔΘΦΜρΘΫ)
Θ®3Θ©AE4÷–A‘≠Ή”‘”Μ·ΙλΒάΖΫ ΫΈΣ:________‘”Μ·ΘΜΤδΙΧΧ§ΨßΧεάύ–ΆΈΣ_______
Θ®4Θ©FΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ______ΘΜœρFΒΡΝρΥα―Έ÷–÷πΒΈΦ”»κΑ±Υ°œ»≤ζ…ζ≥ΝΒμΘ§Κσ≥ΝΒμ»ήΫβΈΣ…νάΕ…Ϊ»ή“ΚΘ§Φ”»κ““¥ΦΜαΈω≥ωάΕ…ΪΨßΧεΘ§ΗΟΨßΧε÷–F”κNH3÷°ΦδΒΡΜ·―ßΦϋΈΣ_______
Θ®5Θ©«βΜ·ΈοΒΡΖ–ΒψΘΚB±»DΗΏΒΡ‘≠“ρ______;
Θ®6Θ©‘ΣΥΊXΒΡΡ≥ΦέΧ§“θάκΉ”Xn-÷–Υυ”–ΒγΉ”’ΐΚΟ≥δ¬ζKΚΆLΒγΉ”≤ψΘ§CnXΨßΧεΒΡΉν–ΓΫαΙΙΒΞ‘Σ»γΆΦΥυ ΨΓΘ
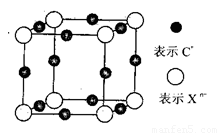
ΗΟΨßΧε÷–―τάκΉ”ΚΆ“θάκΉ”Ηω ΐ±»ΈΣ_______Θ§ΨßΧε÷–ΟΩΗωXn-±Μ_____ΗωΒ»ΨύάκΒΡC+άκΉ”ΑϋΈßΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com