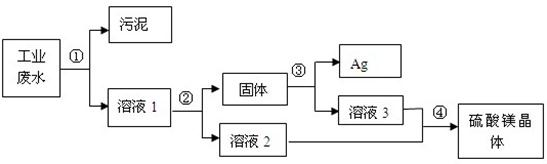
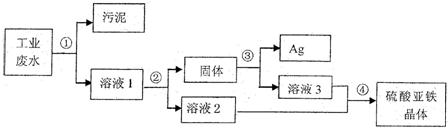
£®2008?ÀÞ«®£©”–“ª÷÷𧓵∑œÀÆ£¨∆‰÷–∫¨”–¥Û¡øµƒ¡ÚÀ·—«Ã˙£¨…Ÿ¡øµƒ“¯¿Î◊”“‘º∞Œ€ƒý£Æƒ≥Õ¨—߅˺∆¡À“ª∏ˆº»æ≠º√”÷∫œ¿Ìµƒ∑Ω∑®ªÿ ’“¯∫Õ¡ÚÀ·—«Ã˙æßãÆ∑Ω∞∏¡˜≥ûÁœ¬£∫

ªÿ¥œ¬¡–Œ £∫
£®1£©≤Ω÷Ë¢⁄÷–£∫–˺”»ÎµƒŒÔ÷ «
Fe
Fe
£¨∑÷¿ÎÀ˘µ√ªÏ∫œŒÔµƒ∑Ω∑® «
π˝¬À
π˝¬À
£Æ
£®2£©≤Ω÷Ë¢€÷–£∫–˺”»ÎµƒŒÔ÷ «
œ°¡ÚÀ·
œ°¡ÚÀ·
£¨∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «
Fe+H2SO4=FeSO4+H2°¸
Fe+H2SO4=FeSO4+H2°¸
£Æ
£®3£©ƒ≥Õ¨—ß»œŒ™æ≠π˝≤Ω÷Ë¢⁄∫ÛÀ˘µ√πÃÃÂæÕ «¥ø檵ƒ“¯£¨≤ª–Ë“™Ω¯––≤Ω÷Ë¢€£¨ƒ„»œŒ™ «∑Ò∫œ¿Ì£ø
≤ª∫œ¿Ì
≤ª∫œ¿Ì
£¨¿Ì”… «
πAg+ÕÍ»´÷√ªª≥ˆ¿¥£¨±ÿ–κ”»Îπ˝¡øµƒÃ˙
πAg+ÕÍ»´÷√ªª≥ˆ¿¥£¨±ÿ–κ”»Îπ˝¡øµƒÃ˙
£Æ
£®4£©≤Ω÷ˢеƒ≤Ÿ◊˜ «
’Ù∑¢Ω·æß
’Ù∑¢Ω·æß
£¨»Ð“∫2∫ջГ∫3Œ™ ≤√¥“™ªÏ∫œ£ø
¡Ω÷÷¬À“∫÷–∂º∫¨”–¡ÚÀ·—«Ã˙£¨ø…µ√µΩ∏¸∂ýµƒ¡ÚÀ·—«Ã˙£¨◊€∫œ¿˚”√
¡Ω÷÷¬À“∫÷–∂º∫¨”–¡ÚÀ·—«Ã˙£¨ø…µ√µΩ∏¸∂ýµƒ¡ÚÀ·—«Ã˙£¨◊€∫œ¿˚”√
£Æ